・平成30年(ワ)第38508号 特許権侵害差止等請求事件(B事件)
・令和3年3月30日判決言渡
・東京地方裁判所民事第47部 田中孝一 横山真通 西尾信員
・A事件及びB事件原告:東レ株式会社
・A事件被告:沢井製薬株式会社、ニプロ株式会社
・B事件被告:扶桑薬品工業株式会社
・特許3531170
・発明の名称:止痒剤
今回は、レミッチ®OD錠(一般名:ナルフラフィン塩酸塩)の後発品に対する侵害訴訟です。
原告の東レは、レミッチOD錠の用途特許である特許3531170の特許権者です。
東レは、レミッチ®カプセル2.5µg、レミッチ®OD錠2.5µgを販売しています。
A事件被告の沢井製薬は、後発品として、ナルフラフィン塩酸塩OD錠2.5µg『サワイ』を販売しています。
B事件被告の扶桑薬品工業は、後発品として、ナルフラフィン塩酸塩OD錠2.5µg『フソー』を販売しています。
本件訴訟は、東レが、後発品の製造販売等の差止め及び廃棄を求めるとともに、不法行為に基づき、沢井製薬に対しては損害金6億2210万円の一部請求として1000万円及びその遅延損害金の、扶桑薬品工業に対しては損害金3億2105万円の一部請求として1000万円及びその遅延損害金の、各支払を求めた事案です。
本件特許の請求項1は以下の通りです。
【請求項1】
下記一般式(I)
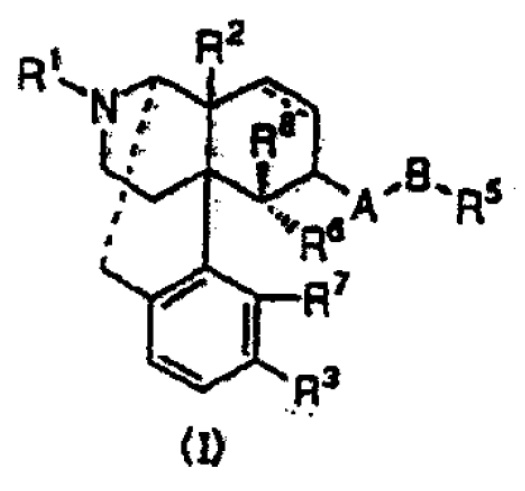
[式中,
・・・(省略)
を表し,R8は水素,炭素数1から5のアルキルまたは炭素数1から5のアルカノイルを表す。また,一般式(I)は(+)体,(-)体,(±)体を含む]で表されるオピオイドκ受容体作動性化合物を有効成分とする止痒剤。
本件特許は延長登録がされており、別途、延長登録の無効審決の取消訴訟の判決が令和3年3月25日に知財高裁から言い渡されています(令和2年(行ケ)第10098号 審決取消請求事件)。本訴訟の判決言渡の5日前です。下記一般式(I)

[式中,
・・・(省略)
を表し,R8は水素,炭素数1から5のアルキルまたは炭素数1から5のアルカノイルを表す。また,一般式(I)は(+)体,(-)体,(±)体を含む]で表されるオピオイドκ受容体作動性化合物を有効成分とする止痒剤。
詳細は前回のブログに記載しています。

<知財高裁/レミッチ用途特許の延長登録無効審決の取消訴訟> 有効成分はナルフラフィンのフリー体、ナルフラフィン塩酸塩の双方であると判断された事例
判決紹介
・令和2年(行ケ)第10098号 審決取消請求事件
・令和3年3月25日判決言渡
・知的財産高等裁判所第2部 森義之 眞鍋美穂子 熊谷大輔
・原告:東レ株式会社
・被告:沢井製薬株式会社、ニプロ株式会社
・特許3...
本件訴訟の争点は、以下の通りです。
(1)被告ら製剤は本件化合物であるナルフラフィン(フリー体)を「有効成分」とするものか
(2)被告ら製剤は本件発明に記載された構成と均等なものか
(3)本件発明は進歩性を欠き無効にされるべきものか
(4)本件延長登録出願により存続期間が延長されたものとみなされた本件特許権の効力は被告ら製剤の製造販売等に及ぶか
(5)本件延長登録出願に基づく延長登録は無効ないし一部無効にされるべきものか
(6)原告による本件特許権の行使は権利濫用となるか
(7)先使用権の存否
(8)損害の額
上記の審決取消訴訟と同じく、「有効成分」の解釈が争点に絡んできています。
裁判所は、争点(1)、(2)について判断しました。抜粋を以下に記載します。
判決(東京地裁)
第3 当裁判所の判断
・・・
1 争点(被告ら製剤は本件化合物であるナルフラフィン(フリー体)を「有効成分」とするものか)について
(1)前記前提事実(3)アのとおり,本件発明の特許請求の範囲は「一般式(Ⅰ) で表されるオピオイドκ受容体作動性化合物を有効成分とする止痒剤」というものであり,本件発明は「止痒剤」という医薬品の製剤を組成する「有効成分」に関する発明であるところ,本件特許権に関する特許公報(甲2)に掲載された本件明細書の記載内容を見ても,この構成要件Aの「有効成分」という用語について特段の定義をした記載は見当たらない。そうすると,本件発明において,この「有効成分」という用語は,医薬品の分野における当業者が理解する通常の意味で用いられているというべきである。そこで,以下,同用語の意味を明らかにするべく,医薬品に関する文献等の記載について検討する。
(2)後記括弧内掲記の証拠等によれば,医薬品に関する文献等において,医薬品の製剤の「有効成分」について,次のとおり記述されていることが認められる。
ア 「active constituent 有効成分 医薬品の組成は有効成分とその他の成分に分けられる。有効成分は薬の効果(たとえば鎮痛)をもたらすものであり,その他の成分(たとえば色素,香料,甘味剤,充塡剤)は,その 有効成分を患者が服用しやすい医薬品(製剤)に仕上げるものである。」(「英和・和英 医薬実用英語ハンドブック」。乙イ15)
イ 「有効成分 薬剤に含有される成分の中で薬効を示す成分のこと。飲みやすくする矯味薬,形状をととのえる賦形剤は含まれない。」(「医薬実務用語集 第9版」。乙イ14)。
ウ 「医薬品の有効成分である原薬は,そのほとんどが固体の結晶として単 離され,医薬品(製剤)開発に供されるが,一概に結晶といっても,低分子原薬が取り得る形態は様々であり,単一結晶であるフリー体,あるいは複合結晶である水和物,溶媒和物,塩および共結晶,さらにそれぞれの結晶多形が存在する可能性があり,多くの候補形態の中から開発に最適な原薬形態すなわち開発形態を選択することが望ましい。開発形態を探索する ために候補化合物の原薬形態スクリーニングを実施し,それにより見出された複数の候補形態の中から良好な物性と安定性を有する原薬形態を選択し,その後の製剤開発を進めるのが製薬企業で実施されている一般的なアプローチである。」,「医薬品の原薬形態とは,有効成分である原薬の固体状態を表現する用語であり,(中略)同一の有効成分であっても様々な 形態を取り得ることが想像されるが,(中略)実際に利用されている原薬形態のうち,単一成分の結晶であるフリー体あるいは複合成分の結晶である水和物および塩が大勢を占めている。」(「ファインケミカルシリーズ 医薬品原薬の結晶化と物性評価:その最先端技術と評価の実際」の「第1編」の「第4章 原薬の開発形態検討」。甲95)
エ 「添加剤は,製剤に含まれる有効成分以外の物質で,有効成分及び製剤の有用性を高める,製剤化を容易にする,品質の安定化を図る,又は使用性を向上させるなどの目的で用いられる。製剤には,必要に応じて,適切な添加剤を加えることができる。」(「第十七改正日本薬局方」(平成28年3月7日厚生労働省告示第64号)の製剤総則の[1]製剤 )
(3)これらの記述によれば,医薬品の分野において,製剤は,主に単一成分の結晶であるフリー体又は複合成分の結晶である水和物及び塩の形態をとっている原薬を有効成分として,これに,色素,香料,甘味剤,充塡剤,矯味薬,賦形剤などの添加剤を加えて組成されたものをいうと認められる。
そうすると,「止痒剤」という製剤を組成する「有効成分」に関する発明である本件明細書の記載に接した当業者としては,通常,この構成要件Aの「有効成分」とは,添加剤を加えて製剤として組成される基となる原薬のことをいうものと理解するといえ,同「有効成分」との文言については,同様の意義を有するものと解するのが相当である。
これを被告ら製剤についてみると,証拠(甲A1,甲B1)によれば,被告ら製剤はいずれもナルフラフィン塩酸塩を原薬として,これに添加剤としてアスパルテーム(L-フェニルアラニン化合物),結晶セルロース,トレハロース,ヒドロキシプロピルセルロース及びL-ロイシンを加えて組成されたものであると認められるから,被告ら製剤において構成要件Aの「有効成分」に当たるものは,本件化合物であるナルフラフィン(フリー体)ではなく,その酸付加塩であるナルフラフィン塩酸塩であるというべきである。
(4)これに対し,原告は,構成要件Aの「有効成分」とは,体内で吸収されて薬理作用を奏する部分を意味し,被告ら製剤においては,ナルフラフィン(フリー体)がこれに当たる旨主張し,その添付文書にも「ナルフラフィン塩酸塩2.5㎍(ナルフラフィンとして2.32㎍)」というようにフリー体が併記されていることを指摘し,上記主張に沿う説明や用例が記載された文献(甲74,75,77ないし88)を提出している。
しかしながら,上記説示のように,当業者は,通常,構成要件Aの「有効成分」とは,添加剤を加えて製剤として組成される基となる原薬のことをいうものと理解するのであって,構成要件Aの「有効成分」との文言は,同様の意義を有するものと解されるところ,被告ら製剤において,投与前の医薬品に含まれているのがナルフラフィン塩酸塩であると認められる以上,被告ら製剤において,ナルフラフィン(フリー体)が構成要件Aの「有効成分」に当たるとはいえない。また,添付文書の上記括弧書き中の記載(「ナルフラフィン塩酸塩2.5㎍(ナルフラフィンとして2.32㎍)」という記載)に接した当業者においては,構成要件Aの「有効成分」について上記の理解に基づいて当該記載を見るのであるから,被告ら製剤において同「有効成分」に当たるものは,ナルフラフィン塩酸塩であると理解するというべきである。さらに,原告の主張に沿う上記の説明や用例は,製剤に関するものとはいえない(甲74,75,77,78)か,製剤に関するものといえるとしても,製剤の組成について述べたものとはいえない(甲79ないし88)から,前記(3)の判断を左右するものではない。
(5)したがって,被告ら製剤は,本件化合物であるナルフラフィン(フリー体)を「有効成分」とするものとは認められず,構成要件Aを充足しないこととなる。
2 争点(2)(被告ら製剤は本件発明に記載された構成と均等なものか)について
(1)前記1で判示したとおり,被告ら製剤はナルフラフィン塩酸塩を有効成分とするものであることから,本件発明と被告ら製剤とは,本件発明に記載された構成を有する止痒剤が本件化合物を有効成分とするものであるのに対し,被告ら製剤は本件化合物の酸付加塩であるナルフラフィン塩酸塩を有効成分とするものである点において相違することとなる。
・・・
これらによれば,出願人たる原告は,本件特許出願時に,本件化合物の薬理学的に許容される酸付加塩を有効成分とする構成を容易に想到することができたにもかかわらず,これを特許請求の範囲に記載しなかったものであるといえ,しかも,客観的,外形的にみて,上記構成が本件発明に記載された構成(本件化合物を有効成分とする構成)を代替すると認識しながらあえて特許請求の範囲に記載しなかった旨を表示していたといえるものというべきである。
そうすると,本件発明については,本件化合物の酸付加塩であるナルフラフィン塩酸塩を有効成分とする被告ら製剤が,本件特許出願の手続において特許請求の範囲から意識的に除外されたものに当たるなどの,被告ら製剤と本件発明に記載された構成(本件化合物を有効成分とする構成)とが均等なものといえない特段の事情が存するというべきである。
(4)したがって,被告ら製剤は,本件発明に記載された構成と均等なものとして,本件発明の技術的範囲に属するということはできない。これに反する原告の主張は,上記説示に照らし,採用の限りでない。
3 結語
以上によれば,被告ら製剤は,本件化合物であるナルフラフィン(フリー体)を「有効成分」とするものとは認められず,構成要件Aを充足しないこととなり,また,本件発明に記載された構成と均等なものとして,本件発明の技術的範囲に属するということもできない。原告は,その他縷々主張するが,その主張内容に照らしてこれらを慎重に精査しても,そのいずれについても,上記説示を左右するに足りるものはない。
よって,その余の争点について判断するまでもなく,原告の請求はいずれも理由がないから,これらを棄却することとして,主文のとおり判決する。
・・・
1 争点(被告ら製剤は本件化合物であるナルフラフィン(フリー体)を「有効成分」とするものか)について
(1)前記前提事実(3)アのとおり,本件発明の特許請求の範囲は「一般式(Ⅰ) で表されるオピオイドκ受容体作動性化合物を有効成分とする止痒剤」というものであり,本件発明は「止痒剤」という医薬品の製剤を組成する「有効成分」に関する発明であるところ,本件特許権に関する特許公報(甲2)に掲載された本件明細書の記載内容を見ても,この構成要件Aの「有効成分」という用語について特段の定義をした記載は見当たらない。そうすると,本件発明において,この「有効成分」という用語は,医薬品の分野における当業者が理解する通常の意味で用いられているというべきである。そこで,以下,同用語の意味を明らかにするべく,医薬品に関する文献等の記載について検討する。
(2)後記括弧内掲記の証拠等によれば,医薬品に関する文献等において,医薬品の製剤の「有効成分」について,次のとおり記述されていることが認められる。
ア 「active constituent 有効成分 医薬品の組成は有効成分とその他の成分に分けられる。有効成分は薬の効果(たとえば鎮痛)をもたらすものであり,その他の成分(たとえば色素,香料,甘味剤,充塡剤)は,その 有効成分を患者が服用しやすい医薬品(製剤)に仕上げるものである。」(「英和・和英 医薬実用英語ハンドブック」。乙イ15)
イ 「有効成分 薬剤に含有される成分の中で薬効を示す成分のこと。飲みやすくする矯味薬,形状をととのえる賦形剤は含まれない。」(「医薬実務用語集 第9版」。乙イ14)。
ウ 「医薬品の有効成分である原薬は,そのほとんどが固体の結晶として単 離され,医薬品(製剤)開発に供されるが,一概に結晶といっても,低分子原薬が取り得る形態は様々であり,単一結晶であるフリー体,あるいは複合結晶である水和物,溶媒和物,塩および共結晶,さらにそれぞれの結晶多形が存在する可能性があり,多くの候補形態の中から開発に最適な原薬形態すなわち開発形態を選択することが望ましい。開発形態を探索する ために候補化合物の原薬形態スクリーニングを実施し,それにより見出された複数の候補形態の中から良好な物性と安定性を有する原薬形態を選択し,その後の製剤開発を進めるのが製薬企業で実施されている一般的なアプローチである。」,「医薬品の原薬形態とは,有効成分である原薬の固体状態を表現する用語であり,(中略)同一の有効成分であっても様々な 形態を取り得ることが想像されるが,(中略)実際に利用されている原薬形態のうち,単一成分の結晶であるフリー体あるいは複合成分の結晶である水和物および塩が大勢を占めている。」(「ファインケミカルシリーズ 医薬品原薬の結晶化と物性評価:その最先端技術と評価の実際」の「第1編」の「第4章 原薬の開発形態検討」。甲95)
エ 「添加剤は,製剤に含まれる有効成分以外の物質で,有効成分及び製剤の有用性を高める,製剤化を容易にする,品質の安定化を図る,又は使用性を向上させるなどの目的で用いられる。製剤には,必要に応じて,適切な添加剤を加えることができる。」(「第十七改正日本薬局方」(平成28年3月7日厚生労働省告示第64号)の製剤総則の[1]製剤 )
(3)これらの記述によれば,医薬品の分野において,製剤は,主に単一成分の結晶であるフリー体又は複合成分の結晶である水和物及び塩の形態をとっている原薬を有効成分として,これに,色素,香料,甘味剤,充塡剤,矯味薬,賦形剤などの添加剤を加えて組成されたものをいうと認められる。
そうすると,「止痒剤」という製剤を組成する「有効成分」に関する発明である本件明細書の記載に接した当業者としては,通常,この構成要件Aの「有効成分」とは,添加剤を加えて製剤として組成される基となる原薬のことをいうものと理解するといえ,同「有効成分」との文言については,同様の意義を有するものと解するのが相当である。
これを被告ら製剤についてみると,証拠(甲A1,甲B1)によれば,被告ら製剤はいずれもナルフラフィン塩酸塩を原薬として,これに添加剤としてアスパルテーム(L-フェニルアラニン化合物),結晶セルロース,トレハロース,ヒドロキシプロピルセルロース及びL-ロイシンを加えて組成されたものであると認められるから,被告ら製剤において構成要件Aの「有効成分」に当たるものは,本件化合物であるナルフラフィン(フリー体)ではなく,その酸付加塩であるナルフラフィン塩酸塩であるというべきである。
(4)これに対し,原告は,構成要件Aの「有効成分」とは,体内で吸収されて薬理作用を奏する部分を意味し,被告ら製剤においては,ナルフラフィン(フリー体)がこれに当たる旨主張し,その添付文書にも「ナルフラフィン塩酸塩2.5㎍(ナルフラフィンとして2.32㎍)」というようにフリー体が併記されていることを指摘し,上記主張に沿う説明や用例が記載された文献(甲74,75,77ないし88)を提出している。
しかしながら,上記説示のように,当業者は,通常,構成要件Aの「有効成分」とは,添加剤を加えて製剤として組成される基となる原薬のことをいうものと理解するのであって,構成要件Aの「有効成分」との文言は,同様の意義を有するものと解されるところ,被告ら製剤において,投与前の医薬品に含まれているのがナルフラフィン塩酸塩であると認められる以上,被告ら製剤において,ナルフラフィン(フリー体)が構成要件Aの「有効成分」に当たるとはいえない。また,添付文書の上記括弧書き中の記載(「ナルフラフィン塩酸塩2.5㎍(ナルフラフィンとして2.32㎍)」という記載)に接した当業者においては,構成要件Aの「有効成分」について上記の理解に基づいて当該記載を見るのであるから,被告ら製剤において同「有効成分」に当たるものは,ナルフラフィン塩酸塩であると理解するというべきである。さらに,原告の主張に沿う上記の説明や用例は,製剤に関するものとはいえない(甲74,75,77,78)か,製剤に関するものといえるとしても,製剤の組成について述べたものとはいえない(甲79ないし88)から,前記(3)の判断を左右するものではない。
(5)したがって,被告ら製剤は,本件化合物であるナルフラフィン(フリー体)を「有効成分」とするものとは認められず,構成要件Aを充足しないこととなる。
2 争点(2)(被告ら製剤は本件発明に記載された構成と均等なものか)について
(1)前記1で判示したとおり,被告ら製剤はナルフラフィン塩酸塩を有効成分とするものであることから,本件発明と被告ら製剤とは,本件発明に記載された構成を有する止痒剤が本件化合物を有効成分とするものであるのに対し,被告ら製剤は本件化合物の酸付加塩であるナルフラフィン塩酸塩を有効成分とするものである点において相違することとなる。
・・・
これらによれば,出願人たる原告は,本件特許出願時に,本件化合物の薬理学的に許容される酸付加塩を有効成分とする構成を容易に想到することができたにもかかわらず,これを特許請求の範囲に記載しなかったものであるといえ,しかも,客観的,外形的にみて,上記構成が本件発明に記載された構成(本件化合物を有効成分とする構成)を代替すると認識しながらあえて特許請求の範囲に記載しなかった旨を表示していたといえるものというべきである。
そうすると,本件発明については,本件化合物の酸付加塩であるナルフラフィン塩酸塩を有効成分とする被告ら製剤が,本件特許出願の手続において特許請求の範囲から意識的に除外されたものに当たるなどの,被告ら製剤と本件発明に記載された構成(本件化合物を有効成分とする構成)とが均等なものといえない特段の事情が存するというべきである。
(4)したがって,被告ら製剤は,本件発明に記載された構成と均等なものとして,本件発明の技術的範囲に属するということはできない。これに反する原告の主張は,上記説示に照らし,採用の限りでない。
3 結語
以上によれば,被告ら製剤は,本件化合物であるナルフラフィン(フリー体)を「有効成分」とするものとは認められず,構成要件Aを充足しないこととなり,また,本件発明に記載された構成と均等なものとして,本件発明の技術的範囲に属するということもできない。原告は,その他縷々主張するが,その主張内容に照らしてこれらを慎重に精査しても,そのいずれについても,上記説示を左右するに足りるものはない。
よって,その余の争点について判断するまでもなく,原告の請求はいずれも理由がないから,これらを棄却することとして,主文のとおり判決する。
注目点としては、被告の製剤が、ナルフラフィン(フリー体)を「有効成分」とするものとは認められないと判断された点です。
これは、上記の延長登録の審決取消訴訟(令和2年(行ケ)第10098号、知財高裁)とは異なる判断です。
延長登録の審決取消訴訟では、裁判所は医薬品の「有効成分」に関して以下のように判断していました。
判決(審決取消訴訟/知財高裁)
オ 以上のことを考え併せると,本件処分の対象となった本件医薬品の有効成分は,先行処分に係る製造販売承認書に記載された「ナルフラフィン塩酸塩」と形式的に決するのではなく,実質的には,本件医薬品の承認審査において,効能,効果を生ぜしめる成分として着目されていたフリー体の「ナルフラフィン」と,本件医薬品に配合されている,その原薬形態の「ナルフラフィン塩酸塩」の双方であると認めるのが相当である。
したがって,「ナルフラフィン塩酸塩」のみを本件医薬品の有効成分と解し,「ナルフラフィン」は,本件医薬品の有効成分ではないと認定して,本件発明の実施に本件処分を受けることが必要であったとはいえないと判断した本件審決の認定判断は誤りであり,取消事由1は理由がある。
したがって,「ナルフラフィン塩酸塩」のみを本件医薬品の有効成分と解し,「ナルフラフィン」は,本件医薬品の有効成分ではないと認定して,本件発明の実施に本件処分を受けることが必要であったとはいえないと判断した本件審決の認定判断は誤りであり,取消事由1は理由がある。
人によって、場面によって解釈が変わりそうな用語なので、判断する裁判所も大変ですね。
次回、知財高裁はどのように判断するのでしょうか。
(判決文PDFはこちら)
コメント