・審判請求日:2017/01/16
・審決日:2020/07/14
・審判官:滝口尚良 穴吹智子 井上典之
・請求人:沢井製薬 株式会社
・参加人:日新製薬 株式会社等
・被請求人:ワーナー-ランバート カンパニー リミテッド ライアビリティー カンパニー
・特許3693258(満了:2022/07/16)
・発明の名称:イソブチルGABAまたはその誘導体を含有する鎮痛剤
無効審判の請求人は沢井製薬で、後発品メーカー15社が参加人になっています。
本件特許の特許査定時の請求項1~4は以下のとおりです。
【請求項1】
式I
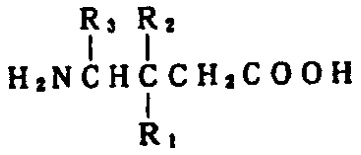
(式中、R1は炭素原子1~6個の直鎖状または分枝状アルキルであり、R2は水素またはメチルであり、R3は水素、メチルまたはカルボキシルである)の化合物またはその医薬的に許容される塩、ジアステレオマー、もしくはエナンチオマーを含有する痛みの処置における鎮痛剤。
【請求項2】
化合物が、式IにおいてR3およびR2はいずれも水素であり、R1は-(CH2)0-2-iC4H9である化合物の(R)、(S)、または(R,S)異性体である請求項1記載の鎮痛剤。
【請求項3】
化合物が、(S)-3-(アミノメチル)-5-メチルヘキサン酸または3-アミノメチル-5-メチルヘキサン酸である請求項1記載の鎮痛剤。
【請求項4】
痛みが炎症性疼痛、神経障害による痛み、癌による痛み、術後疼痛、幻想肢痛、火傷痛、痛風の痛み、骨関節炎の痛み、三叉神経痛の痛み、急性ヘルペスおよびヘルペス後の痛み
、カウザルギーの痛み、特発性の痛み、または線維筋痛症である請求項1記載の鎮痛剤。
式I
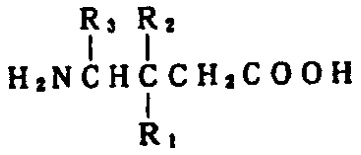
(式中、R1は炭素原子1~6個の直鎖状または分枝状アルキルであり、R2は水素またはメチルであり、R3は水素、メチルまたはカルボキシルである)の化合物またはその医薬的に許容される塩、ジアステレオマー、もしくはエナンチオマーを含有する痛みの処置における鎮痛剤。
【請求項2】
化合物が、式IにおいてR3およびR2はいずれも水素であり、R1は-(CH2)0-2-iC4H9である化合物の(R)、(S)、または(R,S)異性体である請求項1記載の鎮痛剤。
【請求項3】
化合物が、(S)-3-(アミノメチル)-5-メチルヘキサン酸または3-アミノメチル-5-メチルヘキサン酸である請求項1記載の鎮痛剤。
【請求項4】
痛みが炎症性疼痛、神経障害による痛み、癌による痛み、術後疼痛、幻想肢痛、火傷痛、痛風の痛み、骨関節炎の痛み、三叉神経痛の痛み、急性ヘルペスおよびヘルペス後の痛み
、カウザルギーの痛み、特発性の痛み、または線維筋痛症である請求項1記載の鎮痛剤。
請求項1~4の医薬用途について、審判中に、訂正の請求がされました。概要は下記の通りです。審決は、請求項2は新規事項で訂正が認められず、請求項1は一体的に認められないと判断しました。請求項3、4の訂正は認めました。
(×)請求項1:痛覚過敏又は接触異痛の痛み
(×)請求項2:神経障害又は繊維筋痛症による、痛覚過敏又は接触異痛の痛みの処置における
(○)請求項3:炎症を原因とする痛み、又は手術を原因とする痛みの処置における
(○)請求項4:炎症性疼痛による痛覚過敏の痛み、又は術後疼痛による痛覚過敏若しくは接触異痛の痛みの処置における
以下に、請求項2の訂正に関する審決の抜粋を記載します。
審決(訂正)
3 訂正の適否
事案に鑑み、まず、訂正事項2について検討し、順次、訂正事項1、3,4について検討する。
(1)訂正事項2について
訂正事項2に係る訂正は、請求項2において、
式Iの構造式を追加し(訂正事項2-1)、
「請求項1記載の鎮痛剤」、すなわち「痛みの処置における鎮痛剤」を、「神経障害又は繊維筋痛症による、痛覚過敏又は接触異痛の痛みの処置における鎮痛剤」(訂正事項2-2)に訂正するとともに、
請求項1との引用関係を解消し、独立形式に改めることを求めるものである。
ア 特許第36983258号の設定登録時の明細書(以下、「本件特許明細書」という。)及び図面には、上記訂正事項2-2に係る「神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置における」鎮痛作用に関連して以下の記載がある。
・・・
(イ)「本発明は、以下の式Iの化合物の、痛みの処置とくに慢性の疼痛性障害の処置における使用方法である。このような障害にはそれらに限定されるものではないが炎症性疼痛、術後疼痛、転移癌に伴う骨関節炎の痛み、三叉神経痛、急性疱疹性および治療後神経痛、糖尿病性神経障害、カウザルギー、上腕神経叢捻除、後頭部神経痛、反射交感神経ジストロフィー、線維筋痛症、痛風、幻想肢痛、火傷痛ならびに他の形態の神経痛、神経障害および特発性疼痛症候群が包含される。
・・・
(エ)「本発明は、上記式Iの化合物の上に掲げた痛みの処置における鎮痛剤としての使用方法である。痛みにはとくに炎症性疼痛、神経障害の痛み、癌の痛み、術後疼痛、および原因不明の痛みである特発性疼痛たとえば幻想肢痛が包含される。神経障害性の痛みは末梢知覚神経の傷害または感染によって起こる。これには以下に限定されるものではないが、末梢神経の外傷、ヘルペスウイルス感染、糖尿病、カウザルギー、神経叢捻除、神経腫、四肢切断、および血管炎からの痛みが包含される。神経障害性の痛みはまた、慢性アルコール症、ヒト免疫不全ウイルス感染、甲状腺機能低下症、尿毒症またはビタミン欠乏からの神経障害によっても起こる。神経障害性の痛みには、神経傷害によって起こる痛みに限らず、たとえば糖尿病による痛みも包含される。」(特許公報p3 45行~p4 3行)
・・・
イ 摘示(イ)、(エ)には、本件特許明細書記載の発明が、式Iの化合物を線維筋痛症や神経障害等の痛みの処置における鎮痛剤としての使用方法に係る発明であるとの記載がある。そして、摘示(イ)によれば、請求項2記載の化合物は、上記式Iの好ましい化合物とされている。そうすると、本件特許明細書の発明の詳細な説明には、請求項2記載の化合物を線維筋痛症や神経障害等の痛みの処置における鎮痛剤として使用する方法について一般的な記載がなされているといえる。しかし、同化合物を神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置における鎮痛剤として使用することについて明示の記載はない。
本件特許明細書には、末梢神経障害の2つの動物モデルについての説明があるものの(摘示(キ))、請求項2記載の化合物や、該化合物を含む式Iの化合物について、上記モデル試験を行った等、神経障害又は繊維筋痛症による、痛覚過敏又は接触異痛の痛みの処置において鎮痛作用を有し、鎮痛剤としての効果を奏したことを具体的に確認した試験結果はおろか、上記試験において有効であるとの一般的な記載もない。
また、摘示(カ)の記載によれば、本件特許明細書には、請求項2記載の化合物に該当するCI-1008及び3-アミノメチル-5-メチル-ヘキサン酸を用いたラットホルマリン足蹠試験結果、並びに、CI-1008を用いたラットカラゲニン誘発機械的痛覚過敏及び熱痛覚過敏に対する試験結果が記載され、摘示(ク)の記載によれば、請求項2記載の化合物に該当するS-(+)-3-イソブチルギャバを用いたラット術後疼痛モデルにおける熱痛覚過敏及び接触異痛に対する試験結果が記載されている。なお、摘示(ウ)の記載によれば、上記CI-1008は、(S)-3-(アミノメチル)-5-メチルヘキサン酸なる名称の化合物であり、その名称から把握される化学構造からみて、上記S-(+)-3-イソブチルギャバと同じものであると認められる。
しかし、上記試験結果は、いずれも神経障害又は線維筋痛症による痛みの処置に請求項2記載の化合物を使用した試験に関するものではないから、上記試験結果から直ちに、請求項2記載の化合物が、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に有効であることが本件特許明細書に記載されているとはいえない。
そこで、上記した具体的な試験及び試験結果、並びに本件特許出願時の技術常識についてさらに進んで検討し、請求項2記載の化合物が、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に有効であることが本件特許明細書の記載及び技術常識から記載されているに等しいといえるか否かについて検討する。
(ア)ラットホルマリン足蹠試験について
・・・
(ア)-3
以上によれば、本件特許出願時の技術常識を参酌しても、本件特許明細書に、3-アミノメチル-5-メチル-ヘキサン酸及びCI-1008が、ホルマリン足蹠試験の後期相の中等度のブロックを生じたことが記載されていることをもって、請求項2記載の化合物に該当する上記化合物が、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に鎮痛剤として有効であることが記載されているに等しいと当業者が理解するということはできない。
・・・
(イ)ラットカラゲニン誘発機械的痛覚過敏及び熱痛覚過敏に対する試験について
(イ)-3
したがって、本件特許出願時の技術常識を参酌しても、本件特許明細書に、CI-1008がカラゲニン誘発機械的痛覚過敏及び熱痛覚過敏に拮抗したことが記載されていることをもって、請求項2記載の化合物に該当する上記化合物が神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に鎮痛剤として有効であることが記載されているに等しいと当業者が理解するということはできない。
・・・
(ウ)ラット術後疼痛モデルにおける熱痛覚過敏及び接触異痛に対する試験について
(ウ)-3
したがって、本件特許出願時の技術常識を参酌しても、本件特許明細書に、CI-1008がラット術後疼痛モデルにおける熱痛覚過敏及び接触異痛の発生及び維持を遮断したことが記載されていることをもって、請求項2記載の化合物に該当する上記化合物が、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に鎮痛剤として有効であることが記載されているに等しいと当業者が理解するということはできない。
(エ)
以上によれば、訂正事項2は、
式I
・・・
(式I中、R3およびR2はいずれも水素であり、R1は-(CH2)0-2-iC4H9である)の化合物の(R)、(S)、または(R,S)異性体を含有する痛みの処置における鎮痛剤について、その痛みを、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛み、と特定することによって、本件特許明細書又は図面の明示的に記載された事項であるとも、本件特許明細書又は図面の記載から自明な事項であるとも認めることができない痛みに個別化するものであり、該訂正事項に係る訂正は、本件特許明細書の全ての記載を総合しても導き出すことができない技術的事項を含むものであるから、訂正事項2に係る訂正は、本件特許明細書又は図面に記載した事項との関係において、新たな技術的事項を導入するものであると認める。
ウ したがって、訂正事項2-2に係る訂正は、本件特許明細書又は図面に記載した事項の範囲内においてするものであるとはいえない。
事案に鑑み、まず、訂正事項2について検討し、順次、訂正事項1、3,4について検討する。
(1)訂正事項2について
訂正事項2に係る訂正は、請求項2において、
式Iの構造式を追加し(訂正事項2-1)、
「請求項1記載の鎮痛剤」、すなわち「痛みの処置における鎮痛剤」を、「神経障害又は繊維筋痛症による、痛覚過敏又は接触異痛の痛みの処置における鎮痛剤」(訂正事項2-2)に訂正するとともに、
請求項1との引用関係を解消し、独立形式に改めることを求めるものである。
ア 特許第36983258号の設定登録時の明細書(以下、「本件特許明細書」という。)及び図面には、上記訂正事項2-2に係る「神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置における」鎮痛作用に関連して以下の記載がある。
・・・
(イ)「本発明は、以下の式Iの化合物の、痛みの処置とくに慢性の疼痛性障害の処置における使用方法である。このような障害にはそれらに限定されるものではないが炎症性疼痛、術後疼痛、転移癌に伴う骨関節炎の痛み、三叉神経痛、急性疱疹性および治療後神経痛、糖尿病性神経障害、カウザルギー、上腕神経叢捻除、後頭部神経痛、反射交感神経ジストロフィー、線維筋痛症、痛風、幻想肢痛、火傷痛ならびに他の形態の神経痛、神経障害および特発性疼痛症候群が包含される。
・・・
(エ)「本発明は、上記式Iの化合物の上に掲げた痛みの処置における鎮痛剤としての使用方法である。痛みにはとくに炎症性疼痛、神経障害の痛み、癌の痛み、術後疼痛、および原因不明の痛みである特発性疼痛たとえば幻想肢痛が包含される。神経障害性の痛みは末梢知覚神経の傷害または感染によって起こる。これには以下に限定されるものではないが、末梢神経の外傷、ヘルペスウイルス感染、糖尿病、カウザルギー、神経叢捻除、神経腫、四肢切断、および血管炎からの痛みが包含される。神経障害性の痛みはまた、慢性アルコール症、ヒト免疫不全ウイルス感染、甲状腺機能低下症、尿毒症またはビタミン欠乏からの神経障害によっても起こる。神経障害性の痛みには、神経傷害によって起こる痛みに限らず、たとえば糖尿病による痛みも包含される。」(特許公報p3 45行~p4 3行)
・・・
イ 摘示(イ)、(エ)には、本件特許明細書記載の発明が、式Iの化合物を線維筋痛症や神経障害等の痛みの処置における鎮痛剤としての使用方法に係る発明であるとの記載がある。そして、摘示(イ)によれば、請求項2記載の化合物は、上記式Iの好ましい化合物とされている。そうすると、本件特許明細書の発明の詳細な説明には、請求項2記載の化合物を線維筋痛症や神経障害等の痛みの処置における鎮痛剤として使用する方法について一般的な記載がなされているといえる。しかし、同化合物を神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置における鎮痛剤として使用することについて明示の記載はない。
本件特許明細書には、末梢神経障害の2つの動物モデルについての説明があるものの(摘示(キ))、請求項2記載の化合物や、該化合物を含む式Iの化合物について、上記モデル試験を行った等、神経障害又は繊維筋痛症による、痛覚過敏又は接触異痛の痛みの処置において鎮痛作用を有し、鎮痛剤としての効果を奏したことを具体的に確認した試験結果はおろか、上記試験において有効であるとの一般的な記載もない。
また、摘示(カ)の記載によれば、本件特許明細書には、請求項2記載の化合物に該当するCI-1008及び3-アミノメチル-5-メチル-ヘキサン酸を用いたラットホルマリン足蹠試験結果、並びに、CI-1008を用いたラットカラゲニン誘発機械的痛覚過敏及び熱痛覚過敏に対する試験結果が記載され、摘示(ク)の記載によれば、請求項2記載の化合物に該当するS-(+)-3-イソブチルギャバを用いたラット術後疼痛モデルにおける熱痛覚過敏及び接触異痛に対する試験結果が記載されている。なお、摘示(ウ)の記載によれば、上記CI-1008は、(S)-3-(アミノメチル)-5-メチルヘキサン酸なる名称の化合物であり、その名称から把握される化学構造からみて、上記S-(+)-3-イソブチルギャバと同じものであると認められる。
しかし、上記試験結果は、いずれも神経障害又は線維筋痛症による痛みの処置に請求項2記載の化合物を使用した試験に関するものではないから、上記試験結果から直ちに、請求項2記載の化合物が、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に有効であることが本件特許明細書に記載されているとはいえない。
そこで、上記した具体的な試験及び試験結果、並びに本件特許出願時の技術常識についてさらに進んで検討し、請求項2記載の化合物が、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に有効であることが本件特許明細書の記載及び技術常識から記載されているに等しいといえるか否かについて検討する。
(ア)ラットホルマリン足蹠試験について
・・・
(ア)-3
以上によれば、本件特許出願時の技術常識を参酌しても、本件特許明細書に、3-アミノメチル-5-メチル-ヘキサン酸及びCI-1008が、ホルマリン足蹠試験の後期相の中等度のブロックを生じたことが記載されていることをもって、請求項2記載の化合物に該当する上記化合物が、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に鎮痛剤として有効であることが記載されているに等しいと当業者が理解するということはできない。
・・・
(イ)ラットカラゲニン誘発機械的痛覚過敏及び熱痛覚過敏に対する試験について
(イ)-3
したがって、本件特許出願時の技術常識を参酌しても、本件特許明細書に、CI-1008がカラゲニン誘発機械的痛覚過敏及び熱痛覚過敏に拮抗したことが記載されていることをもって、請求項2記載の化合物に該当する上記化合物が神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に鎮痛剤として有効であることが記載されているに等しいと当業者が理解するということはできない。
・・・
(ウ)ラット術後疼痛モデルにおける熱痛覚過敏及び接触異痛に対する試験について
(ウ)-3
したがって、本件特許出願時の技術常識を参酌しても、本件特許明細書に、CI-1008がラット術後疼痛モデルにおける熱痛覚過敏及び接触異痛の発生及び維持を遮断したことが記載されていることをもって、請求項2記載の化合物に該当する上記化合物が、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛みの処置に鎮痛剤として有効であることが記載されているに等しいと当業者が理解するということはできない。
(エ)
以上によれば、訂正事項2は、
式I
・・・
(式I中、R3およびR2はいずれも水素であり、R1は-(CH2)0-2-iC4H9である)の化合物の(R)、(S)、または(R,S)異性体を含有する痛みの処置における鎮痛剤について、その痛みを、神経障害又は線維筋痛症による、痛覚過敏又は接触異痛の痛み、と特定することによって、本件特許明細書又は図面の明示的に記載された事項であるとも、本件特許明細書又は図面の記載から自明な事項であるとも認めることができない痛みに個別化するものであり、該訂正事項に係る訂正は、本件特許明細書の全ての記載を総合しても導き出すことができない技術的事項を含むものであるから、訂正事項2に係る訂正は、本件特許明細書又は図面に記載した事項との関係において、新たな技術的事項を導入するものであると認める。
ウ したがって、訂正事項2-2に係る訂正は、本件特許明細書又は図面に記載した事項の範囲内においてするものであるとはいえない。
争点は、実施可能要件、サポート要件です。
裁判所は、請求項3、4は実施可能要件、サポート要件を満たすが、請求項1、2は満たさないと判断しました。
これで後発品が承認されることが予想されます。とはいってもまだわかりませんので、今後の動向を要チェックです。 また、審決を読むと、薬理試験結果がけっこう厳密に求められています。
上位概念の医薬用途を有効に取得するのはなかなか大変ですね。下位概念疾患に関しても機序が異なると同様です。
この観点でもインパクトのある審決です。知財高裁はどのように判断するのでしょうか(提起されれば)。
以下に、請求項1、2の実施可能要件に関する審決の抜粋を記載します。
審決(実施可能要件)
第7 当合議体の判断
当合議体は、本件発明3、4の特許についての無効理由1及び2は理由がない、本件発明1~2の特許は、無効理由1及び2によって無効にすべきものである、と判断する。その理由は、以下のとおりである。
1 無効理由1(実施可能要件違反)について
(1)特許法第36条第4項に規定する要件について
ア 平成14年法律第24号による改正前の特許法第36条第4項の規定によれば、発明の詳細な説明は,通商産業省令で定めるところにより、その発明の属する技術分野における通常の知識を有する者がその実施をすることができる程度に明確かつ十分に、記載しなければならない、との要件、いわゆる実施可能要件に適合するものでなければならない。そして、該実施可能要件における「実施」には、物の発明の場合、特許法第2条第3項第1号に規定する「その物の使用をする行為」が含まれる。
そうすると、発明の詳細な説明の記載が、物の発明について、実施可能要件を満たすためには、その発明の属する技術の分野における通常の知識を有する者がその物の使用をすることができる程度のものである必要がある。
イ ここで、上記物の発明が、ある物質の未知の属性に基づき当該物質の新たな医薬用途を提供しようとする物の発明(いわゆる医薬用途発明)である場合について検討する。
医薬の技術分野においては、現在でも、物質の名称や化学構造だけからその未知の医薬用途を予測することは困難であり、何らかの薬理試験結果によらなければその物質の新たな医薬用途を認識することができない、という事情が存在する。
したがって、医薬の技術分野における上記事情に鑑みれば、発明の詳細な説明の記載が、医薬用途発明を使用することができる程度のものであるといえるためには、薬理試験結果によらずとも、その未知の医薬用途を予測することができる物質を用いているなどの特段の事情でもない限り、発明の詳細な説明に、当該物質が実際にその医薬用途の対象疾患に対して治療効果を有することを当業者が認識することができるに足る薬理試験結果を記載する必要がある。
ウ 本件発明は、第3で説示したとおりの鎮痛剤の発明であり、特許請求の範囲に記載される化合物(以下、総称して、「本件化合物」、又は、各々請求項を区別して、「請求項1記載の化合物」~「請求項4記載の化合物」という。)の、未知の属性に基づき、当該化合物の新たな
「痛みの処置における鎮痛」
という請求項1、2に記載の医薬用途や、該痛みの具体例といえる、
「炎症を原因とする痛み、又は手術を原因とする痛みの処置における鎮痛」
という請求項3に記載の医薬用途、
及び
「炎症性疼痛による痛覚過敏の痛み、又は術後疼痛による痛覚過敏若しくは接触異痛の痛みの処置における鎮痛」
という請求項4に記載の医薬用途
を提供しようとする物の発明(いわゆる医薬用途発明)である。
ところで、請求項1記載の化合物である式Iの化合物が鎮痛剤として使用される痛みについて、本件特許明細書の発明の詳細な説明に、「炎症性疼痛、術後疼痛、転移癌に伴う骨関節炎の痛み、三叉神経痛、急性疱疹性および治療後神経痛、糖尿病性神経障害、カウザルギー、上腕神経叢捻除、後頭部神経痛、反射交感神経ジストロフィー、線維筋痛症、痛風、幻想肢痛、火傷痛ならびに他の形態の神経痛、神経障害および特発性疼痛症候群」が包含されると記載されていることに照らせば(前記第2 3(1)の摘示(イ))、上記請求項1に記載の医薬用途には、上記痛みの処置における鎮痛を含むものである。
そして、本件化合物に、薬理試験結果によらずとも、その未知の医薬用途を予測することができる物質であるといった、特段の事情は見いだせないから、本件特許明細書の発明の詳細な説明の記載が、本件発明を使用することができる程度のものであるといえるためには、本件特許明細書の発明の詳細な説明に、本件発明1にあっては、請求項1記載の化合物が、少なくとも上記明細書の発明の詳細な説明に記載の各痛みの処置における鎮痛効果を、本件発明2にあっては、請求項2記載の化合物が少なくとも上記明細書の発明の詳細な説明に記載されている各痛みの処置における鎮痛効果を、そして、本件発明3及び4にあっては、各々、請求項3、4記載の化合物が、請求項3、4に記載の痛みの処置における鎮痛効果を有することを、当業者が認識することができるに足る薬理試験結果を記載する必要がある。
エ そこで進んで、上記薬理試験結果の記載について検討するに、当該薬理試験が、医薬用途発明における医薬用途の対象疾患を有する患者に対して行った臨床試験であり、当該疾患に対する治療効果が認められる試験結果が得られたというのであれば、当業者は、当該医薬用途発明が実際にその医薬用途の対象疾患に対して治療効果を有することを認識することができる。
また、当該薬理試験が、動物実験や試験管内実験といった非臨床試験であっても、当業者が技術常識を踏まえてその結果を見ると、医薬用途発明における医薬用途の対象疾患に対する治療効果があると認識することができる試験であれば足りる。ここで、上記技術常識は、発明の詳細な説明の記載が実施可能要件を満たすか否かを検討すべき特許出願の出願時のものである。
オ 以上のア~エの説示に照らして、本件特許明細書の発明の詳細な説明の記載について、本件特許出願時の技術常識を踏まえて、以下、検討する。
(2)検討
ア 本件特許明細書の発明の詳細な説明には、本件発明の鎮痛剤が上記痛みに対する治療効果を有することについて、前記第2 3(1)アに摘示したとおり、摘示(ア)~(ク)の記載がある。
イ 摘示(オ)の記載によれば、本件特許明細書の発明の詳細な説明には、本件発明の鎮痛剤の有効量、投与方法、製剤化のための事項が記載されている。加えて、摘示(カ)の記載によれば、本件化合物に該当するCI-1008及び3-アミノメチル-5-メチル-ヘキサン酸を用いたラットホルマリン足蹠試験結果、並びに、CI-1008を用いたラットカラゲニン痛覚過敏に対する試験結果が記載され、摘示(ク)の記載によれば、本件化合物に該当するS-(+)-3-イソブチルギャバを用いたラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験結果が記載されている。なお、摘示(ウ)の記載によれば、上記CI-1008は、(S)-3-(アミノメチル)-5-メチルヘキサン酸なる名称の化合物であり、その名称から把握される化学構造からみて、上記S-(+)-3-イソブチルギャバと同じものであると認められる。
そして、その他の記載事項をあわせみるに、本件特許明細書の発明の詳細な説明の記載は、上記薬理試験結果に基づき、本件化合物が、特許請求の範囲に記載されている各痛みや摘示(イ)をはじめとする種々の種類の痛みの治療に有効であることを当業者に認識させようとするものであるといえる。
ウ そこで、当業者が本件特許出願時の技術常識を踏まえて上記薬理試験結果を見ると、本件化合物に特許請求の範囲や摘示(イ)に記載されている各痛みに対する治療効果があると認識することができるか否か検討する。
事案に鑑み、まず、請求項3に記載の痛みに対する治療効果について、次に請求項4に記載の痛みに対する治療効果について検討する。
・・・
オ 次に、請求項1、2に記載の痛みに対する治療効果について検討する。
(ア)請求項1には、痛みとの記載があるにとどまり、該痛みに関して具体的な記載はなされていない。一方、本件特許明細書の発明の詳細な説明には、式Iの化合物をその処置に用いる痛みに関連して、「炎症性疼痛、術後疼痛、転移癌に伴う骨関節炎の痛み、三叉神経痛、急性疱疹性および治療後神経痛、糖尿病性神経障害、カウザルギー、上腕神経叢捻除、後頭部神経痛、反射交感神経ジストロフィー、線維筋痛症、痛風、幻想肢痛、火傷痛ならびに他の形態の神経痛、神経障害および特発性疼痛症候群」が包含される、と記載されているから(摘示(イ))、請求項1の痛みは、具体例として、少なくとも、上記本件特許明細書の発明の詳細な説明に具体的に記載されている各痛みを包含するものであるといえる。そこで、以下においては、請求項1に包含される上記本件特許明細書の発明の詳細な説明に記載されている各痛みに対する治療効果について検討する。
まず、上記本件特許明細書の発明の詳細な説明に記載されている各痛みについては、その原因や病態生理はさまざまで、治療法も異なることが、例えば、甲第3~5、7~9、14、18及び19号証に記載されている(摘示事項3A~3E、4A、4B、5A~5E、7A、8A、9A~9G、14A、18A~18C、19A、19B)。そして、甲第3号証は、著名な医学辞典であるから、当業者の技術常識を認定する基礎として適切なものである(なお、甲第3号証の奥付のページの記載によれば、甲第3号証の書籍は、その第2版第2刷として1997年7月20日に発行されたものであるが、その第2版第1刷は、本件特許出願前の1996年3月31日に発行されたものであり、通常、同じ版であれば内容は変わらないから、甲第3号証は、本件特許出願時の当業者の技術常識を認定する基礎として適切なものである。)。また、甲第4、5、7~9、14、18及び19号証は、本件特許出願前に頒布された書籍であって、その書籍名からみて、医学の教科書又は臨床医療者の知見といえる書籍であると推認され、それら書籍の記載事項は、当業者の誰もが習得又は知得しているべきものであるから、当業者の技術常識を認定する基礎として適切なものである。
そうすると、痛みには、本件特許明細書の発明の詳細な説明に記載されている各痛みを含む種々の種類のものがあり、その原因や病態生理もさまざまであることは、本件特許出願時の技術常識であったものと認められる。また、痛みの種類や原因によって治療法が異なり、鎮痛剤であればあらゆる種類の痛みに有効であるというわけではないことも、本件特許出願時の技術常識であったものと認められる。
(イ)そして、上記各甲号証及び各乙号証の記載を見ても、ラットホルマリン足蹠試験、ラットカラゲニン誘発痛覚過敏に対する試験、または、ラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験という3種の薬理試験において上記のような結果が得られれば、上記「炎症性疼痛」及び「術後疼痛」以外の本件特許明細書に記載されている各痛みの治療に有効であるという、本件特許出願時の技術常識は見いだせない。
(ウ)請求項2記載の化合物は、請求項1記載の化合物である式Iの化合物に包含されるものであり、該化合物を用いる痛みの処置についても、前記(ア)と同様に判断される。
(エ)したがって、当業者は、本件特許明細書の発明の詳細な説明に記載の上記3種の薬理試験結果の記載に接しても、本件発明1、2に係る鎮痛剤が、「炎症性疼痛」及び「術後疼痛」以外の本件特許明細書に記載されている各痛みの処置における鎮痛効果を有することを認識することができない。
カ 被請求人の主張について
(ア)被請求人は、平成29年4月27日付け答弁書p5 11行~p8 6行、同p9 10行~p11下から5行及び令和1年7月1日付け上申書p17下から10行~p27 5行において、本件特許明細書の発明の詳細な説明に記載の上記3種の薬理試験について、以下のa及びbの主張をしている。
a ラットホルマリン足蹠試験について
1)乙第4、20、22~28号証によれば、ホルマリン疼痛モデルのlate phaseは、脊髄後角における神経細胞の発火および痛覚過敏に関連した、疼痛モデルとして認識されていた。
2)甲第6号証によれば、神経障害性疼痛である上腕神経叢捻除、ヘルペス後神経痛(帯状疱疹後神経痛)および幻想肢痛において、脊髄後角における神経細胞の異常発火や過敏性が報告されている。
3)乙第2、3号証によれば、痛覚過敏のような痛覚・知覚異常は、神経障害性疼痛や線維筋痛症に共通する痛みである。
4)以上から、当業者は、ホルマリン疼痛モデルに対する効果から、本件化合物が神経障害性疼痛や線維筋痛症に効果を有することを予測することができる。
b ラットカラゲニン誘発痛覚過敏に対する試験、及び、ラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験について
1)本件特許明細書の発明の詳細な説明には、カラゲニン疼痛モデルは、痛覚・知覚異常の症状である、機械的痛覚過敏および熱痛覚過敏を呈する実験動物モデルであると記載されている。
2)本件特許明細書の発明の詳細な説明には、術後疼痛モデルは、痛覚・知覚異常の症状である、熱痛覚過敏および接触異痛を呈する実験動物モデルであると記載されている。
3)乙第2、3号証によれば、痛覚過敏のような痛覚・知覚異常は、神経障害性疼痛や線維筋痛症に共通する痛みである。
4)よって、当業者は、カラゲニン疼痛モデルに対する効果や術後疼痛モデルに対する効果から、本件化合物が神経障害性疼痛や線維筋痛症に効果を有することを予測することができる。
(イ)そこで上記主張について検討する。
a ラットホルマリン足蹠試験について
まず第一に、ホルマリン疼痛モデルのlate phaseは、脊髄後角における神経細胞の発火および痛覚過敏に関連した疼痛モデルとして認識されていた、という技術常識が本件特許出願時に存在していたことを証する証拠として、被請求人は、乙第4号証、乙第22~25号証、乙第28号証を提示する。
乙第4号証には、ホルマリン試験について、「動物における侵害刺激のモデルとして使用されてきている。」(摘示事項乙4A)ことが記載されており、一方、late phaseと痛覚過敏の関連については、「痛覚過敏の主要な機序がlate phaseの一因でもあるかもしれない。」(摘示事項乙4C)という推測が記載されているにすぎない。そうすると、乙第4号証の記載内容が技術常識の根拠であるという前提に立ったとしても、ホルマリン疼痛モデルのlate phaseは脊髄後角における神経細胞の発火および痛覚過敏に関連した、疼痛モデルとして認識されていた、という技術常識が本件特許出願時に存在していたとはいえない。
また、乙第22~25号証、乙第28号証には、前記第2 3(1)イ(ア)-2で説示したとおりの記載があり、それら記載によれば、ホルマリン足蹠試験の後期相における反応と中枢性感作との関係は未だ仮説又は推論の域にとどまるものと理解されるのであって、本件特許出願時、ホルマリン足蹠試験の後期相における反応が、中枢性感作等の痛みの処置における何らかの特性やメカニズムに基づくものであるとか、それらを反映した結果であり、それら特性やメカニズムの関与を証明するための確立された試験であるとの技術常識が存在していたと認めることはできず、また、ホルマリン足蹠試験が、末梢及び中枢神経の過敏の痛み全般についての試験であるとの技術常識が存在していたともいえないことは、前記第2 3(1)イ(ア)-2で説示したとおりである。
以上によれば、本件特許出願時、上記1)のような認識が存在していたとはいえず、たとえ、上記2)、3)で主張するように、それら痛みに痛覚過敏がみられるとしても、本件特許明細書の発明の詳細な説明に、3-アミノメチル-5-メチル-ヘキサン酸及びCI-1008が、ホルマリン足蹠試験の後期相の中等度のブロックを生じたことが記載されていることをもって、請求項1又は2記載の化合物に該当する上記化合物が、神経障害性疼痛や線線維筋痛症の痛みの処置における鎮痛剤として有効であることが記載されているに等しいと当業者が理解するということはできない。
また、仮に、上記1)のような認識が本件特許出願時に存在していたとしても、その一方で、オの項で説示したとおり、痛みの種類によって治療法が異なり、鎮痛剤であればあらゆる種類の痛みに有効であるというわけではないという技術常識も本件特許出願時に存在していたのであるから、痛みというものに、脊髄後角における神経細胞の発火や痛覚過敏を呈するという共通点があったとしても、痛みの種類や原因によって薬の効き方に差が出るであろうと当業者は認識していたものと認められる。そうすると、3-アミノメチル-5-メチル-ヘキサン酸及びCI-1008を用いたラットホルマリン足蹠試験の結果に基づき、ホルマリンがその誘発原因であるとはいえない神経障害性疼痛や線維筋痛症にも効果を有することを、当業者が予測することができたとはいえない。
b ラットカラゲニン誘発痛覚過敏に対する試験、及び、ラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験について
前記オの項で説示したとおり、痛みの種類によって治療法が異なり、鎮痛剤であればあらゆる種類の痛みに有効であるというわけではないという技術常識が本件特許出願時存在していたのであるから、痛みというものに、痛覚・知覚異常の症状である、機械的痛覚過敏および熱痛覚過敏や、熱痛覚過敏および接触異痛を呈するという共通点があったとしても、痛みの種類や原因によって薬の効き方に差が出るであろうと当業者は認識していたものと認められる。そうすると、CI-1008を用いたラットカラゲニン誘発痛覚過敏に対する試験やラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験の結果に基づき、カラゲニンや足蹠筋肉の切開創がその誘発原因であるとはいえない神経障害性疼痛や線維筋痛症にも効果を有することを、当業者が予測することができたとはいえない。
(ウ)ほかにも、被請求人は、本件特許明細書の発明の詳細な説明を見た当業者が上記「炎症性疼痛」及び「術後疼痛」以外の、訂正前の請求項4に記載の各痛み、すなわち、摘示(イ)又は(エ)に記載の各痛みの治療に本件化合物が有効であると認識することができる理由として、以下のa~dの主張をしているので、各々、検討する。
・・・
当合議体は、本件発明3、4の特許についての無効理由1及び2は理由がない、本件発明1~2の特許は、無効理由1及び2によって無効にすべきものである、と判断する。その理由は、以下のとおりである。
1 無効理由1(実施可能要件違反)について
(1)特許法第36条第4項に規定する要件について
ア 平成14年法律第24号による改正前の特許法第36条第4項の規定によれば、発明の詳細な説明は,通商産業省令で定めるところにより、その発明の属する技術分野における通常の知識を有する者がその実施をすることができる程度に明確かつ十分に、記載しなければならない、との要件、いわゆる実施可能要件に適合するものでなければならない。そして、該実施可能要件における「実施」には、物の発明の場合、特許法第2条第3項第1号に規定する「その物の使用をする行為」が含まれる。
そうすると、発明の詳細な説明の記載が、物の発明について、実施可能要件を満たすためには、その発明の属する技術の分野における通常の知識を有する者がその物の使用をすることができる程度のものである必要がある。
イ ここで、上記物の発明が、ある物質の未知の属性に基づき当該物質の新たな医薬用途を提供しようとする物の発明(いわゆる医薬用途発明)である場合について検討する。
医薬の技術分野においては、現在でも、物質の名称や化学構造だけからその未知の医薬用途を予測することは困難であり、何らかの薬理試験結果によらなければその物質の新たな医薬用途を認識することができない、という事情が存在する。
したがって、医薬の技術分野における上記事情に鑑みれば、発明の詳細な説明の記載が、医薬用途発明を使用することができる程度のものであるといえるためには、薬理試験結果によらずとも、その未知の医薬用途を予測することができる物質を用いているなどの特段の事情でもない限り、発明の詳細な説明に、当該物質が実際にその医薬用途の対象疾患に対して治療効果を有することを当業者が認識することができるに足る薬理試験結果を記載する必要がある。
ウ 本件発明は、第3で説示したとおりの鎮痛剤の発明であり、特許請求の範囲に記載される化合物(以下、総称して、「本件化合物」、又は、各々請求項を区別して、「請求項1記載の化合物」~「請求項4記載の化合物」という。)の、未知の属性に基づき、当該化合物の新たな
「痛みの処置における鎮痛」
という請求項1、2に記載の医薬用途や、該痛みの具体例といえる、
「炎症を原因とする痛み、又は手術を原因とする痛みの処置における鎮痛」
という請求項3に記載の医薬用途、
及び
「炎症性疼痛による痛覚過敏の痛み、又は術後疼痛による痛覚過敏若しくは接触異痛の痛みの処置における鎮痛」
という請求項4に記載の医薬用途
を提供しようとする物の発明(いわゆる医薬用途発明)である。
ところで、請求項1記載の化合物である式Iの化合物が鎮痛剤として使用される痛みについて、本件特許明細書の発明の詳細な説明に、「炎症性疼痛、術後疼痛、転移癌に伴う骨関節炎の痛み、三叉神経痛、急性疱疹性および治療後神経痛、糖尿病性神経障害、カウザルギー、上腕神経叢捻除、後頭部神経痛、反射交感神経ジストロフィー、線維筋痛症、痛風、幻想肢痛、火傷痛ならびに他の形態の神経痛、神経障害および特発性疼痛症候群」が包含されると記載されていることに照らせば(前記第2 3(1)の摘示(イ))、上記請求項1に記載の医薬用途には、上記痛みの処置における鎮痛を含むものである。
そして、本件化合物に、薬理試験結果によらずとも、その未知の医薬用途を予測することができる物質であるといった、特段の事情は見いだせないから、本件特許明細書の発明の詳細な説明の記載が、本件発明を使用することができる程度のものであるといえるためには、本件特許明細書の発明の詳細な説明に、本件発明1にあっては、請求項1記載の化合物が、少なくとも上記明細書の発明の詳細な説明に記載の各痛みの処置における鎮痛効果を、本件発明2にあっては、請求項2記載の化合物が少なくとも上記明細書の発明の詳細な説明に記載されている各痛みの処置における鎮痛効果を、そして、本件発明3及び4にあっては、各々、請求項3、4記載の化合物が、請求項3、4に記載の痛みの処置における鎮痛効果を有することを、当業者が認識することができるに足る薬理試験結果を記載する必要がある。
エ そこで進んで、上記薬理試験結果の記載について検討するに、当該薬理試験が、医薬用途発明における医薬用途の対象疾患を有する患者に対して行った臨床試験であり、当該疾患に対する治療効果が認められる試験結果が得られたというのであれば、当業者は、当該医薬用途発明が実際にその医薬用途の対象疾患に対して治療効果を有することを認識することができる。
また、当該薬理試験が、動物実験や試験管内実験といった非臨床試験であっても、当業者が技術常識を踏まえてその結果を見ると、医薬用途発明における医薬用途の対象疾患に対する治療効果があると認識することができる試験であれば足りる。ここで、上記技術常識は、発明の詳細な説明の記載が実施可能要件を満たすか否かを検討すべき特許出願の出願時のものである。
オ 以上のア~エの説示に照らして、本件特許明細書の発明の詳細な説明の記載について、本件特許出願時の技術常識を踏まえて、以下、検討する。
(2)検討
ア 本件特許明細書の発明の詳細な説明には、本件発明の鎮痛剤が上記痛みに対する治療効果を有することについて、前記第2 3(1)アに摘示したとおり、摘示(ア)~(ク)の記載がある。
イ 摘示(オ)の記載によれば、本件特許明細書の発明の詳細な説明には、本件発明の鎮痛剤の有効量、投与方法、製剤化のための事項が記載されている。加えて、摘示(カ)の記載によれば、本件化合物に該当するCI-1008及び3-アミノメチル-5-メチル-ヘキサン酸を用いたラットホルマリン足蹠試験結果、並びに、CI-1008を用いたラットカラゲニン痛覚過敏に対する試験結果が記載され、摘示(ク)の記載によれば、本件化合物に該当するS-(+)-3-イソブチルギャバを用いたラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験結果が記載されている。なお、摘示(ウ)の記載によれば、上記CI-1008は、(S)-3-(アミノメチル)-5-メチルヘキサン酸なる名称の化合物であり、その名称から把握される化学構造からみて、上記S-(+)-3-イソブチルギャバと同じものであると認められる。
そして、その他の記載事項をあわせみるに、本件特許明細書の発明の詳細な説明の記載は、上記薬理試験結果に基づき、本件化合物が、特許請求の範囲に記載されている各痛みや摘示(イ)をはじめとする種々の種類の痛みの治療に有効であることを当業者に認識させようとするものであるといえる。
ウ そこで、当業者が本件特許出願時の技術常識を踏まえて上記薬理試験結果を見ると、本件化合物に特許請求の範囲や摘示(イ)に記載されている各痛みに対する治療効果があると認識することができるか否か検討する。
事案に鑑み、まず、請求項3に記載の痛みに対する治療効果について、次に請求項4に記載の痛みに対する治療効果について検討する。
・・・
オ 次に、請求項1、2に記載の痛みに対する治療効果について検討する。
(ア)請求項1には、痛みとの記載があるにとどまり、該痛みに関して具体的な記載はなされていない。一方、本件特許明細書の発明の詳細な説明には、式Iの化合物をその処置に用いる痛みに関連して、「炎症性疼痛、術後疼痛、転移癌に伴う骨関節炎の痛み、三叉神経痛、急性疱疹性および治療後神経痛、糖尿病性神経障害、カウザルギー、上腕神経叢捻除、後頭部神経痛、反射交感神経ジストロフィー、線維筋痛症、痛風、幻想肢痛、火傷痛ならびに他の形態の神経痛、神経障害および特発性疼痛症候群」が包含される、と記載されているから(摘示(イ))、請求項1の痛みは、具体例として、少なくとも、上記本件特許明細書の発明の詳細な説明に具体的に記載されている各痛みを包含するものであるといえる。そこで、以下においては、請求項1に包含される上記本件特許明細書の発明の詳細な説明に記載されている各痛みに対する治療効果について検討する。
まず、上記本件特許明細書の発明の詳細な説明に記載されている各痛みについては、その原因や病態生理はさまざまで、治療法も異なることが、例えば、甲第3~5、7~9、14、18及び19号証に記載されている(摘示事項3A~3E、4A、4B、5A~5E、7A、8A、9A~9G、14A、18A~18C、19A、19B)。そして、甲第3号証は、著名な医学辞典であるから、当業者の技術常識を認定する基礎として適切なものである(なお、甲第3号証の奥付のページの記載によれば、甲第3号証の書籍は、その第2版第2刷として1997年7月20日に発行されたものであるが、その第2版第1刷は、本件特許出願前の1996年3月31日に発行されたものであり、通常、同じ版であれば内容は変わらないから、甲第3号証は、本件特許出願時の当業者の技術常識を認定する基礎として適切なものである。)。また、甲第4、5、7~9、14、18及び19号証は、本件特許出願前に頒布された書籍であって、その書籍名からみて、医学の教科書又は臨床医療者の知見といえる書籍であると推認され、それら書籍の記載事項は、当業者の誰もが習得又は知得しているべきものであるから、当業者の技術常識を認定する基礎として適切なものである。
そうすると、痛みには、本件特許明細書の発明の詳細な説明に記載されている各痛みを含む種々の種類のものがあり、その原因や病態生理もさまざまであることは、本件特許出願時の技術常識であったものと認められる。また、痛みの種類や原因によって治療法が異なり、鎮痛剤であればあらゆる種類の痛みに有効であるというわけではないことも、本件特許出願時の技術常識であったものと認められる。
(イ)そして、上記各甲号証及び各乙号証の記載を見ても、ラットホルマリン足蹠試験、ラットカラゲニン誘発痛覚過敏に対する試験、または、ラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験という3種の薬理試験において上記のような結果が得られれば、上記「炎症性疼痛」及び「術後疼痛」以外の本件特許明細書に記載されている各痛みの治療に有効であるという、本件特許出願時の技術常識は見いだせない。
(ウ)請求項2記載の化合物は、請求項1記載の化合物である式Iの化合物に包含されるものであり、該化合物を用いる痛みの処置についても、前記(ア)と同様に判断される。
(エ)したがって、当業者は、本件特許明細書の発明の詳細な説明に記載の上記3種の薬理試験結果の記載に接しても、本件発明1、2に係る鎮痛剤が、「炎症性疼痛」及び「術後疼痛」以外の本件特許明細書に記載されている各痛みの処置における鎮痛効果を有することを認識することができない。
カ 被請求人の主張について
(ア)被請求人は、平成29年4月27日付け答弁書p5 11行~p8 6行、同p9 10行~p11下から5行及び令和1年7月1日付け上申書p17下から10行~p27 5行において、本件特許明細書の発明の詳細な説明に記載の上記3種の薬理試験について、以下のa及びbの主張をしている。
a ラットホルマリン足蹠試験について
1)乙第4、20、22~28号証によれば、ホルマリン疼痛モデルのlate phaseは、脊髄後角における神経細胞の発火および痛覚過敏に関連した、疼痛モデルとして認識されていた。
2)甲第6号証によれば、神経障害性疼痛である上腕神経叢捻除、ヘルペス後神経痛(帯状疱疹後神経痛)および幻想肢痛において、脊髄後角における神経細胞の異常発火や過敏性が報告されている。
3)乙第2、3号証によれば、痛覚過敏のような痛覚・知覚異常は、神経障害性疼痛や線維筋痛症に共通する痛みである。
4)以上から、当業者は、ホルマリン疼痛モデルに対する効果から、本件化合物が神経障害性疼痛や線維筋痛症に効果を有することを予測することができる。
b ラットカラゲニン誘発痛覚過敏に対する試験、及び、ラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験について
1)本件特許明細書の発明の詳細な説明には、カラゲニン疼痛モデルは、痛覚・知覚異常の症状である、機械的痛覚過敏および熱痛覚過敏を呈する実験動物モデルであると記載されている。
2)本件特許明細書の発明の詳細な説明には、術後疼痛モデルは、痛覚・知覚異常の症状である、熱痛覚過敏および接触異痛を呈する実験動物モデルであると記載されている。
3)乙第2、3号証によれば、痛覚過敏のような痛覚・知覚異常は、神経障害性疼痛や線維筋痛症に共通する痛みである。
4)よって、当業者は、カラゲニン疼痛モデルに対する効果や術後疼痛モデルに対する効果から、本件化合物が神経障害性疼痛や線維筋痛症に効果を有することを予測することができる。
(イ)そこで上記主張について検討する。
a ラットホルマリン足蹠試験について
まず第一に、ホルマリン疼痛モデルのlate phaseは、脊髄後角における神経細胞の発火および痛覚過敏に関連した疼痛モデルとして認識されていた、という技術常識が本件特許出願時に存在していたことを証する証拠として、被請求人は、乙第4号証、乙第22~25号証、乙第28号証を提示する。
乙第4号証には、ホルマリン試験について、「動物における侵害刺激のモデルとして使用されてきている。」(摘示事項乙4A)ことが記載されており、一方、late phaseと痛覚過敏の関連については、「痛覚過敏の主要な機序がlate phaseの一因でもあるかもしれない。」(摘示事項乙4C)という推測が記載されているにすぎない。そうすると、乙第4号証の記載内容が技術常識の根拠であるという前提に立ったとしても、ホルマリン疼痛モデルのlate phaseは脊髄後角における神経細胞の発火および痛覚過敏に関連した、疼痛モデルとして認識されていた、という技術常識が本件特許出願時に存在していたとはいえない。
また、乙第22~25号証、乙第28号証には、前記第2 3(1)イ(ア)-2で説示したとおりの記載があり、それら記載によれば、ホルマリン足蹠試験の後期相における反応と中枢性感作との関係は未だ仮説又は推論の域にとどまるものと理解されるのであって、本件特許出願時、ホルマリン足蹠試験の後期相における反応が、中枢性感作等の痛みの処置における何らかの特性やメカニズムに基づくものであるとか、それらを反映した結果であり、それら特性やメカニズムの関与を証明するための確立された試験であるとの技術常識が存在していたと認めることはできず、また、ホルマリン足蹠試験が、末梢及び中枢神経の過敏の痛み全般についての試験であるとの技術常識が存在していたともいえないことは、前記第2 3(1)イ(ア)-2で説示したとおりである。
以上によれば、本件特許出願時、上記1)のような認識が存在していたとはいえず、たとえ、上記2)、3)で主張するように、それら痛みに痛覚過敏がみられるとしても、本件特許明細書の発明の詳細な説明に、3-アミノメチル-5-メチル-ヘキサン酸及びCI-1008が、ホルマリン足蹠試験の後期相の中等度のブロックを生じたことが記載されていることをもって、請求項1又は2記載の化合物に該当する上記化合物が、神経障害性疼痛や線線維筋痛症の痛みの処置における鎮痛剤として有効であることが記載されているに等しいと当業者が理解するということはできない。
また、仮に、上記1)のような認識が本件特許出願時に存在していたとしても、その一方で、オの項で説示したとおり、痛みの種類によって治療法が異なり、鎮痛剤であればあらゆる種類の痛みに有効であるというわけではないという技術常識も本件特許出願時に存在していたのであるから、痛みというものに、脊髄後角における神経細胞の発火や痛覚過敏を呈するという共通点があったとしても、痛みの種類や原因によって薬の効き方に差が出るであろうと当業者は認識していたものと認められる。そうすると、3-アミノメチル-5-メチル-ヘキサン酸及びCI-1008を用いたラットホルマリン足蹠試験の結果に基づき、ホルマリンがその誘発原因であるとはいえない神経障害性疼痛や線維筋痛症にも効果を有することを、当業者が予測することができたとはいえない。
b ラットカラゲニン誘発痛覚過敏に対する試験、及び、ラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験について
前記オの項で説示したとおり、痛みの種類によって治療法が異なり、鎮痛剤であればあらゆる種類の痛みに有効であるというわけではないという技術常識が本件特許出願時存在していたのであるから、痛みというものに、痛覚・知覚異常の症状である、機械的痛覚過敏および熱痛覚過敏や、熱痛覚過敏および接触異痛を呈するという共通点があったとしても、痛みの種類や原因によって薬の効き方に差が出るであろうと当業者は認識していたものと認められる。そうすると、CI-1008を用いたラットカラゲニン誘発痛覚過敏に対する試験やラット足蹠筋肉切開により生じた熱痛覚過敏及び接触異痛に対する試験の結果に基づき、カラゲニンや足蹠筋肉の切開創がその誘発原因であるとはいえない神経障害性疼痛や線維筋痛症にも効果を有することを、当業者が予測することができたとはいえない。
(ウ)ほかにも、被請求人は、本件特許明細書の発明の詳細な説明を見た当業者が上記「炎症性疼痛」及び「術後疼痛」以外の、訂正前の請求項4に記載の各痛み、すなわち、摘示(イ)又は(エ)に記載の各痛みの治療に本件化合物が有効であると認識することができる理由として、以下のa~dの主張をしているので、各々、検討する。
・・・

コメント
[…] <リリカ特許の無効審判> 医薬用途の訂正及び実施可能要件・サポート要件が認められなかった審決例審決紹介 ・審判番号:無効2017-800003 ・審判請求日:2017/01/16 ・審決日:2020/07/14 […]
[…] <リリカ特許の無効審判> 医薬用途の訂正及び実施可能要件・サポート要件が認められなかった審決例審決紹介 ・審判番号:無効2017-800003 ・審判請求日:2017/01/16 ・審決日:2020/07/14 […]
[…] <リリカ特許の無効審判> 医薬用途の訂正及び実施可能要件・サポート要件が認められなかった審決例審決紹介 ・審判番号:無効2017-800003 ・審判請求日:2017/01/16 ・審決日:2020/07/14 […]