お疲れさまです。
7平日連続で判決紹介の記事を投稿してきましたが、本日で連続投稿は終了します。
この機会にいくつかの判決を分析できてよかったです。
このブログではほとんど取り上げていない医薬・バイオ以外の分野や、外国の判決もできる限り多く把握した方が実務の品質を上げるためにはよいのですが、かなりの量なのでそこは難しい問題です。ウェブサイトや書籍、論文等でまとめられた記事を読むのだけでも相当な時間がかかりますし。もしかしたら、案件をチームでやるっていうのはその解に近いのかもしれませんね。
とりあえずこのブログでは、気軽に書ける医薬・バイオ分野の判決の紹介を中心に今後もやっていくのかなと思います。
今後ともよろしくお願いいたします。
以下、判決紹介です。
・令和2年(行ケ)第10135号 審決取消請求事件
・令和4年3月7日判決言渡
・知的財産高等裁判所第2部 本多知成 浅井憲 中島朋宏
・原告:ワーナー-ランバート カンパニー リミテッド ライアビリティー カンパニー
・被告:沢井製薬株式会社、他15社
・特許3693258
・発明の名称:イソブチルGABAまたはその誘導体を含有する鎮痛剤
ワーナー-ランバート(原告)は、特許3693258の特許権者です。特許3693258はプレガバリン(販売名:リリカカプセル25mg、75mg、150mg)(処分の対象となった物)の製造販売承認に基づいて特許権存続期間の延長登録がされています。延長後の存続期間満了日は2022年7月16日です。
ワーナー-ランバートは、ファイザーに対し本件特許権に係る専用実施権を設定しており、ファイザーはリリカカプセル、リリカOD錠を販売しています。リリカの効能・効果は「神経障害性疼痛、線維筋痛症に伴う疼痛」です。
沢井製薬(被告)は2017年1月16日に特許3693258に対して無効審判を請求し、2020年7月14日に一部無効審決(請求項1、2は無効)が出ていました。これに伴い、2020年8月17日に沢井製薬を含む22社のリリカ後発品が製造販売承認され、2020年12月11日に発売されました。
各社の動き、判決をまとめると以下のようになります。
●2017年1月16日:沢井製薬が無効審判請求(請求人側に15社が参加)
●2020年7月14日:一部無効審決(請求項1、2は無効、請求項3、4は請求不正立)
●2020年8月17日:リリカ後発品の製造販売承認(22社80品目)
●2020年8月17日:ファイザーが侵害訴訟提起のニュースリリース
●2020年11月19日:ワーナー-ランバートが審決取消訴訟を提起
●2020年12月11日:リリカ後発品の薬価収載、発売
●2021年11月24日:侵害訴訟の判決(日本ジェネリックの後発品は非侵害)
●2021年11月30日:侵害訴訟の判決(日新製薬及びMeiji Seikaファルマの後発品は非侵害)
●2021年11月30日:侵害訴訟の判決(共和薬品工業の後発品は非侵害)
●2021年12月10日:侵害訴訟の判決(第一三共エスファ及び第一三共の後発品は非侵害)
●2021年12月23日:侵害訴訟の判決(ニプロ、全星薬品工業及び全星薬品の後発品は非侵害)
●2021年12月23日:侵害訴訟の判決(東和薬品の後発品は非侵害)
●2021年12月24日:侵害訴訟の判決(小林化工の後発品は非侵害)
●2021年12月24日:侵害訴訟の判決(日医工の後発品は非侵害)
●2022年1月19日:侵害訴訟の判決(武田テバファーマ及び武田薬品工業の後発品は非侵害)
●2022年1月19日:侵害訴訟の判決(フェルゼンファーマの後発品は非侵害)
●2022年1月19日:侵害訴訟の判決(日本ケミファ及び日本薬品工業の後発品は非侵害)
●2022年2月2日:侵害訴訟の判決(ダイト及び科研製薬の後発品は非侵害)
●2022年2月16日:侵害訴訟の判決(辰巳化学、陽進堂及び三笠製薬の後発品は非侵害)
●2022年3月7日:審決取消訴訟の判決 ← 今回
このうち、一部無効審決と、小林化工の判決、日新製薬及びMeiji Seikaファルマの判決は下記ブログで紹介しています。

<リリカ特許の無効審判> 医薬用途の訂正及び実施可能要件・サポート要件が認められなかった審決例
審決紹介
・審判番号:無効2017-800003
・審判請求日:2017/01/16
・審決日:2020/07/14
・審判官:滝口尚良 穴吹智子 井上典之
・請求人:沢井製薬 株式会社
・参加人:日新製薬 株式会社等
・...

<東京地裁/リリカ用途特許の侵害訴訟> 「痛みの処置における鎮痛剤」は実施可能要件・サポート要件を満たさないと判断され、訂正も認められなかった事例(ワーナー対小林化工)
判決紹介
・令和2年(ワ)第19927号 特許権侵害差止請求事件
・令和3年12月24日判決言渡
・東京地方裁判所民事第29部 國分隆文 小川暁 佐々木亮
・原告:ワーナー-ランバート カンパニー リミテッド ライアビリティー ...

<東京地裁/リリカ用途特許の侵害訴訟> 明細書に痛みの下位概念を列挙した箇所があっても、下位概念への訂正は新規事項の追加に当たると判断された事例(ワーナー対日新製薬+Meiji Seikaファルマ)
判決紹介
・令和2年(ワ)第19918号 特許権侵害差止請求事件(第1事件)
・同年(ワ)第22291号 特許権侵害差止請求事件(第2事件)
・令和3年11月30日判決言渡
・東京地方裁判所民事第47部 田中孝一 小口五大 鈴木...
今回は、2022年3月7日の「審決取消訴訟」の判決のご紹介です。
まず、本件特許の特許査定時の請求項1~4は以下のとおりです。
【請求項1】
式I
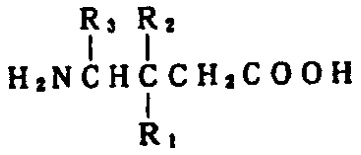
(式中、R1は炭素原子1~6個の直鎖状または分枝状アルキルであり、R2は水素またはメチルであり、R3は水素、メチルまたはカルボキシルである)の化合物またはその医薬的に許容される塩、ジアステレオマー、もしくはエナンチオマーを含有する痛みの処置における鎮痛剤。
【請求項2】
化合物が、式IにおいてR3およびR2はいずれも水素であり、R1は-(CH2)0-2-iC4H9である化合物の(R)、(S)、または(R,S)異性体である請求項1記載の鎮痛剤。
【請求項3】
化合物が、(S)-3-(アミノメチル)-5-メチルヘキサン酸または3-アミノメチル-5-メチルヘキサン酸である請求項1記載の鎮痛剤。
【請求項4】
痛みが炎症性疼痛、神経障害による痛み、癌による痛み、術後疼痛、幻想肢痛、火傷痛、痛風の痛み、骨関節炎の痛み、三叉神経痛の痛み、急性ヘルペスおよびヘルペス後の痛み
、カウザルギーの痛み、特発性の痛み、または線維筋痛症である請求項1記載の鎮痛剤。
審決では、ワーナー-ランバートのした訂正請求に対して、請求項1、2への訂正は新規事項のため認められないと判断されていました。概要は下記の通りです(右側は訂正後の用途です)。式I
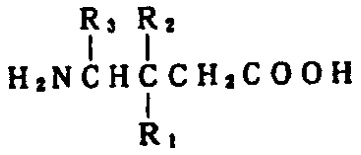
(式中、R1は炭素原子1~6個の直鎖状または分枝状アルキルであり、R2は水素またはメチルであり、R3は水素、メチルまたはカルボキシルである)の化合物またはその医薬的に許容される塩、ジアステレオマー、もしくはエナンチオマーを含有する痛みの処置における鎮痛剤。
【請求項2】
化合物が、式IにおいてR3およびR2はいずれも水素であり、R1は-(CH2)0-2-iC4H9である化合物の(R)、(S)、または(R,S)異性体である請求項1記載の鎮痛剤。
【請求項3】
化合物が、(S)-3-(アミノメチル)-5-メチルヘキサン酸または3-アミノメチル-5-メチルヘキサン酸である請求項1記載の鎮痛剤。
【請求項4】
痛みが炎症性疼痛、神経障害による痛み、癌による痛み、術後疼痛、幻想肢痛、火傷痛、痛風の痛み、骨関節炎の痛み、三叉神経痛の痛み、急性ヘルペスおよびヘルペス後の痛み
、カウザルギーの痛み、特発性の痛み、または線維筋痛症である請求項1記載の鎮痛剤。
(×)請求項1:痛覚過敏又は接触異痛の痛み
(×)請求項2:神経障害又は繊維筋痛症による、痛覚過敏又は接触異痛の痛みの処置における
(○)請求項3:炎症を原因とする痛み、又は手術を原因とする痛みの処置における
(○)請求項4:炎症性疼痛による痛覚過敏の痛み、又は術後疼痛による痛覚過敏若しくは接触異痛の痛みの処置における
また審決では、請求項1、2(訂正前の「痛み」)は実施可能要件、サポート要件を満たさないと判断されていました。
この審決に対して、ワーナー(原告)が審決取消訴訟を提起していました。
そして今回、知財高裁は、本件審決に誤りはないとして、ワーナーの請求を棄却しました。
(訂正と実施可能要件/サポート要件に関する結論は、上の侵害訴訟の判決と同じです。)
知財高裁は、訂正については、
『本件訂正が新規事項の追加に当たらないというためには,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置における鎮痛剤として「効果を奏すること」が本件明細書又は図面に記載されているか,記載されているに等しいと当業者が理解するといえなければならないというべきである。』
と判示しており、実施可能要件については、
『本件化合物が原因を異にするあらゆる「痛み」の処置においても効果を奏すると理解したとは到底いえない。』
と判示しています。
上の侵害訴訟の判決も含め、医薬用途の特許実務において非常に重要な判決ですね。
最後に、判決抜粋を以下に記載しておきます。
判決
第5 当裁判所の判断
1 取消事由1(本件訂正についての判断の誤り)について
(1)訂正の要件(新規事項の追加)について
ア 原告は,本件化合物2につき神経障害や線維筋痛症による痛覚過敏や接触異痛の痛みに対して「効果を奏すること」を当業者が理解できるか否かは実施可能要件等の記載要件に係る判断において検討すべき事柄であるから,本件化合物2につき神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置に鎮痛剤として「有効であること」が記載されているに等しいと当業者が理解するとはいえないとして訂正事項2-2に係る本件訂正が新規事項の追加に当たると判断した本件審決は特許法134条の2第9項において準用する同法126条5項の適用を誤るものであると主張する。
イ 特許無効審判における訂正の請求は,「願書に添付した明細書,特許請求の範囲又は図面に記載した事項の範囲内において」しなければならず(特許法134条の2第9項において準用する同法126条5項),同事項とは,当業者によって,明細書,特許請求の範囲又は図面の全ての記載を総合することにより導かれる技術的事項であり,訂正が,このようにして導かれる技術的事項との関係において,新たな技術的事項を導入しないものであるときは,当該訂正は,いわゆる新規事項の追加とならず,「明細書,特許請求の範囲又は図面に記載した事項の範囲内において」するものということができる(知財高裁平成18年(行ケ)第10563号同20年5月30日判決参照)。
しかるところ,本件発明2は,公知の物質である本件化合物2について鎮痛剤としての医薬用途を見出したとするいわゆる医薬用途発明であるところ,訂正事項2-2に係る本件訂正は,「請求項1記載の(鎮痛剤)」とあるのを「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛みの処置における(鎮痛剤)」に訂正するというものであり,鎮痛剤としての用途を具体的に特定することを求めるものである。そして,「痛みの処置における鎮痛剤」が医薬用途発明たり得るためには,当該鎮痛剤が当該痛みの処置において有効であることが当然に求められるのであるから,訂正事項2-2に係る本件訂正が新規事項の追加に当たらないというためには,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置における鎮痛剤として「効果を奏すること」が,当業者によって,本件出願日当時の技術常識も考慮して,本件明細書(本件訂正前の特許請求の範囲を含む。以下同じ。)又は図面の全ての記載を総合することにより導かれる技術的事項として存在しなければならないことになる。
ウ この点に関し,原告は,新規事項の追加に当たるか否かの判断においては,訂正事項が当業者によって明細書又は図面の全ての記載を総合することにより導かれる技術的事項であるか否かが検討されれば足りることから,本件審決の判断には誤りがあると主張する。しかしながら,上記のとおりの本件発明2の内容及び訂正事項2-2の内容に照らせば,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置に「効果を奏すること」が本件明細書又は図面の記載から導かれなければ,訂正事項2-2につき,これが当業者によって本件明細書又は図面の全ての記載を総合することにより導かれる技術的事項であるとはいえない。したがって,原告の上記主張を前提にしても,訂正事項2-2に係る本件訂正が新規事項の追加に当たらないというためには,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置における鎮痛剤として「効果を奏すること」が本件明細書又は図面に記載されているか,記載されているに等しいと当業者が理解するといえなければならないというべきである。
エ したがって,訂正事項2-2に係る本件訂正が新規事項の追加に当たらないというためには,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置における鎮痛剤として「効果を奏すること」が本件明細書に記載されているか,記載されているに等しいと当業者が理解するといえなければならないというべきであるとした本件審決(なお,本件審決は,本件訂正の許否の判断において,本件明細書に加えて図面の記載についても検討しており,本件審決のいう「明細書」は図面を含む趣旨と解される。)は,特許法134条の2第9項において準用する同法126条5項の適用を誤るものではない。
(2)訂正事項2-2に係る本件訂正が願書に添付した明細書又は図面に記載した事項の範囲内の訂正であるとの原告の主張について
本件審決が判断した順序に従い,まず,訂正事項2-2に係る本件訂正について判断する。
ア 本件化合物2が「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛み」の処置において効果を奏することにつき本件明細書又は図面に明示の記載があるかについて
(ア)本件明細書及び図面の記載
・・・
(イ)検討
a(a)前記(ア)bのとおり,本件明細書には,発明の概要として,本件化合物2が使用される疼痛性障害の中に神経障害及び線維筋痛症が含まれる旨の記載があるが,この部分には,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない(なお,本件化合物2が使用される疼痛性障害の中に神経障害及び線維筋痛症が含まれるとの一般的な記載があっても,そのことから,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏すると解することはできない。)。
(b)前記(ア)cのとおり,本件明細書には,発明の詳述として,本件化合物2が鎮痛剤として使用される対象の痛みに神経障害の痛みが含まれる旨の記載があるが,この部分にも,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない。
(c)前記(ア)dのとおり,本件明細書には,ホルマリン試験に関し,本件化合物2がホルマリン試験の後期相において効果を奏し,初期相においては影響がなかった旨の記載があるが,この部分にも,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない。
(d)前記(ア)eのとおり,本件明細書には,カラゲニン試験に関し,本件化合物2が機械的痛覚過敏及び熱痛覚過敏の痛みに対して効果を奏した旨の記載があるが,この部分にも,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない(なお,本件明細書の当該部分には,本件化合物2が「炎症性疼痛」の処置に有効であることを示す旨の記載がある。)。
(e)前記(ア)gのとおり,本件明細書には,術後疼痛試験に関し,本件化合物2が熱痛覚過敏及び接触異痛の痛みに対して効果を奏した旨の記載があるが,この部分にも,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない。
(f)その他,本件明細書及び図面には,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載がないから,本件明細書及び図面には,その旨の明示の記載がないと認めるのが相当である。
b この点に関し,原告は,本件明細書には,ホルマリン試験において中枢性感作及びこれによる痛覚過敏や接触異痛の痛みを反映する後期相に対する本件化合物2の効果が確かめられている旨,カラゲニン試験において痛覚過敏の痛みに対する本件化合物2の効果が確かめられている旨並びに術後疼痛試験において痛覚過敏及び接触異痛の痛みに対する本件化合物2の効果が確かめられている旨の記載があるから,本件明細書には,本件化合物2を痛覚過敏や接触異痛の痛みに対して用いることも,神経障害性疼痛や線維筋痛症に対して用いることも明示されていると主張する。
しかしながら,ホルマリン試験の後期相が中枢性感作及びこれによる痛覚過敏や接触異痛の痛みを反映するものであることが本件出願日当時の技術常識であったとの原告の主張が認められないことは,後記イ(ア)bにおいて説示するとおりであるし,前記a(c)ないし(e)において説示したところに照らすと,ホルマリン試験,カラゲニン試験及び術後疼痛試験の結果に係る記載を考慮しても,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は線維筋痛症の痛みの処置において効果を奏することが本件明細書又は図面に明示されていると認めることはできない。原告の上記主張は,採用することができない。
イ 本件化合物2が「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛み」の処置において効果を奏することが本件明細書又は図面に記載されているに等しいと本件出願日当時の当業者が理解したといえるかについて
(ア)原告が主張する本件出願日当時の技術常識の存否について
原告は,本件化合物2が「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛み」の処置において効果を奏することが本件明細書に明記されていないとしても,本件出願日当時の技術常識に照らせば,これが記載されているに等しいと当業者は理解したといえるとして,様々な技術常識の存在について主張し,また,これを認定しなかった本件審決が誤りであると主張するので,以下,原告が主張する技術常識の存否について順次検討する。
・・・
(イ)原告が主張する各技術常識が存在しなかったことは,前記(ア)において説示したとおりであるから,これを前提に,本件出願日当時の当業者において,本件化合物2が「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛み」の処置において効果を奏することが本件明細書又は図面に記載されているに等しいと理解したといえるかについて以下検討する。
a 原告は,ホルマリン試験によって引き起こされた後期相に本件化合物2を用いることにより効果が確認された旨の本件明細書の記載を根拠に,痛覚過敏及び接触異痛の痛みの処置に本件化合物2を用いることは,本件明細書の記載から自明であると主張する。
原告の上記主張は,本件出願日当時にホルマリン試験の後期相が中枢性感作によって生じる痛覚過敏及び接触異痛の痛みに対する薬剤の効果を確認する試験として広く知られていたことを根拠とするものである。しかしながら,前記(ア)bにおいて説示したとおり,ホルマリン試験の後期相が専ら中枢性感作を反映したものであることや,ホルマリン試験が痛覚過敏及び接触異痛の痛みに対する薬剤の効果を確認するための試験であることが本件出願日当時の技術常識であったと認めることはできないから,原告の上記主張は,その根拠を欠くものといわざるを得ない。
・・・
ウ 以上のとおりであるから,訂正事項2-2に係る本件訂正が願書に添付した明細書又は図面に記載した事項の範囲内の訂正であるということはできない。したがって,訂正事項2-2に係る本件訂正は,特許法134条の2第9項において準用する同法126条5項に違反し,許されない。
(3)訂正事項2に係る本件訂正について
訂正事項2-2に係る本件訂正が許されないことは,前記(2)において説示したとおりであるから,訂正事項2-2を含む訂正事項2に係る本件訂正も,特許法134条の2第9項において準用する同法126条5項に違反し,許されない。これと同旨の本件審決の判断に誤りはない。
(4)訂正事項1に係る本件訂正について
本件訂正前の請求項1及び2は,請求項2が請求項1の記載を引用する関係にあるから,請求項1及び2に係る本件訂正(訂正事項1及び2に係る本件訂正)は,一群の請求項1及び2についてされるものであるところ,前記(3)において説示したとおり,訂正事項2に係る本件訂正は許されないから,請求項2と共に一群の請求項を構成する請求項1に係る本件訂正(訂正事項1に係る本件訂正)も,許されない。これと同旨の本件審決の判断に誤りはない(なお,原告も,請求項2に係る本件訂正(訂正事項2に係る本件訂正)が許されない場合には,請求項2と共に一群の請求項を構成する請求項1に係る本件訂正(訂正事項1に係る本件訂正)も許されないことになることを争うものではない。)。
(5)小括
以上のとおり,訂正事項1及び2に係る本件訂正を許さなかった本件審決の判断に誤りはない。取消事由1は理由がない。
2 取消事由2(実施可能要件についての判断の誤り)について
(1)平成14年法律第24号による改正前の特許法36条4項は,明細書の発明の詳細な説明は,その発明の属する技術の分野における通常の知識を有する者がその実施をすることができる程度に明確かつ十分に記載しなければならないと定めるところ,この規定にいう「実施」とは,物の発明については,その物の使用等をする行為をいうのであるから(特許法2条3項1号),物の発明について実施可能要件を満たすためには,明細書の発明の詳細な説明の記載が,当業者において,その記載及び出願時の技術常識に基づいて,過度の試行錯誤を要することなく,当該発明に係る物を使用することができる程度のものでなければならない。
そして,医薬用途発明においては,一般に,物質名,化学構造等が示されることのみによっては,その有用性を予測することは困難であり,発明の詳細な説明に,医薬の有効量,投与方法等が記載されていても,それだけでは,当業者において当該医薬が実際にその用途において使用できるかを予測することは困難であるから,当業者が過度の試行錯誤を要することなく当該発明に係る物を使用することができる程度の記載があるというためには,明細書において,当該物質が当該用途に使用できることにつき薬理データ又はこれと同視することができる程度の事項を記載し,出願時の技術常識に照らして,当該物質が当該用途の医薬として使用できることを当業者が理解できるようにする必要があると解するのが相当である。
これを本件についてみると,本件各発明は,前記第2の2のとおり,本件化合物を「痛みの処置における鎮痛剤」の用途に使用する医薬用途発明であるから,本件各発明について本件明細書の発明の詳細な説明の記載が実施可能要件を満たすといえるためには,本件明細書において,本件化合物が「痛みの処置における鎮痛剤」の用途に使用できることにつき薬理データ又はこれと同視することができる程度の事項を記載し,本件出願日当時の技術常識に照らして,本件化合物が当該用途の医薬として使用できることを当業者が理解できるようにする必要がある。
(2)原告は,本件明細書の記載に加え,本件出願日当時の技術常識を併せ考慮すれば,本件明細書の記載を見た当業者は本件化合物が原因にかかわらず痛覚過敏や接触異痛の痛みに対して効果を奏するものと理解し,また,本件化合物が少なくとも神経障害や線維筋痛症による痛覚過敏や接触異痛の痛みに対して効果を奏するものと理解するといえるとして,本件明細書の発明の詳細な説明が本件各発明について実施可能要件を満たすと主張するので,まず,原告が主張する技術常識の存否について,以下検討する(もっとも,前記(1)のとおり,本件各発明は,「痛み」の処置における鎮痛剤の用途に使用されるものであり,当該「痛み」には何らの特定もされていないのであるから,実施可能要件を満たすか否かを判断するに当たって検討すべき本件出願日当時の当業者の理解の対象は,本件化合物が「痛覚過敏や接触異痛の痛み」又は「神経障害や線維筋痛症による痛覚過敏や接触異痛の痛み」に対して効果を奏することではなく,本件化合物が「痛み」に対して効果を奏することである。)。
ア 原告は,神経障害性疼痛や線維筋痛症による痛覚過敏や接触異痛の痛みはその原因にかかわらず抹消や中枢の神経細胞の感作によって生じることが本件出願日当時に知られていたと主張するが,そのような事実が認められないことは,前記1(2)イ(ア)aにおいて説示したとおりである。
なお,原告は,特発性疼痛についても,神経細胞の感作により痛みの症状が生じるものであると主張するが,前記1(2)イ(ア)aにおいて説示したところに照らすと,そのような事実を認めることはできず,その他,そのような事実を認めるに足りる的確な証拠はない。
イ 原告は,中枢性感作に対して効果を奏するケタミンが原因にかかわらず痛覚過敏や接触異痛の痛みに対して効果があることが本件出願日当時に知られていたと主張するが,そのような事実が認められないことは,前記1(2)イ(ア)eにおいて説示したとおりである。
ウ 原告は,上記ア及びイの技術常識が存在したことを根拠に,本件出願日当時の当業者は痛みに共通の治療法があることを理解していたと主張するが,上記ア及びイの技術常識は認められないから,原告の主張は根拠を欠くものとして失当である。
エ 原告は,本件出願日当時,ホルマリン試験の後期相は中枢性感作を反映するものであるとの技術常識が存在し,これは仮説ではなかったと主張するが,ホルマリン試験の後期相が専ら中枢性感作を反映したものであることが技術常識であったと認めることができないことは,前記1(2)イ(ア)bにおいて説示したとおりである。
なお,原告は,カラゲニン試験及び術後疼痛試験についても,神経の機能異常に基づく痛覚過敏や接触異痛の痛みを反映するものであったと主張するが,前記1(2)イ(ア)a及びcにおいて説示したところに照らすと,そのような事実を認めることはできず,その他,そのような事実を認めるに足りる的確な証拠はない。オ原告は,痛みを原因によって区別できないことは本件出願日当時の技術常識であったと主張するが,そのような技術常識が認められないことは,前記1(2)イ(ア)fにおいて説示したとおりである。
カ 原告は,本件出願日当時の当業者は疼痛の原因にかかわらず,痛覚過敏や接触異痛の痛みを発現する動物モデル試験で特定の化合物の効果を確認できれば,その動物モデル試験におけるのとは別の原因によって生じた痛覚過敏や接触異痛の痛みに対しても当該化合物が同様に効果を奏するものと理解していたと主張するが,原告の主張が前提を欠き失当であることは,前記1(2)イ(ア)f(d)において説示したとおりである。
キ なお,原告は,本件明細書においてベネットモデルやチャングモデルへの言及があれば,本件出願日当時の当業者は炎症や手術とは異なる原因によって生じた痛覚過敏や接触異痛の痛みに対しても本件化合物が有用であることを十分に理解できたと主張する。しかしながら,前記1(2)ア(ア)fのとおり,本件明細書には,ベネットモデル及びチャングモデルについて,「BennetG.J.のアッセイはヒトに認められるのと類似の疼痛感覚の障害を生じるラットにおける末梢性単発神経障害の動物モデルを提供する(Pain,1988;33:87-107)。KimS.H.らのアッセイは,ラットにおける分節脊椎神経の結紮によって生じる末梢神経障害の一つの実験モデルを提供する(Pain,1990;50:355-363)。」との記載があるのみであり,本件化合物がベネットモデルやチャングモデルにおいてどのような結果を示したのかについての記載は全くないから,上記記載をもって,本件出願日当時の当業者が炎症や手術とは異なる原因によって生じた痛覚過敏や接触異痛の痛みに対しても本件化合物が有用であることを理解できたと認めることはできない。
この点に関し,原告は,本件出願日後の文献である甲28の文献(Elsevier Science B.V.発行の「pain 83」(1999年)に掲載された「Detection of static and dynamic components of mechanical allodynia in rat models of neuropathic pain: are they signaled by distinct primary sensory neurons?」(Mark J. Fieldら著))の記載は本件化合物が実際にベネットモデルやチャングモデルにおいて効果を奏したことを裏付けるものであるから,これを参酌すべきであると主張するが,上記のとおり,本件明細書には,本件化合物がベネットモデルやチャングモデルにおいて効果を奏した旨の記載が全くないのであるから,甲28の文献の記載が本件明細書の記載内容を裏付けるとはいえない。原告の主張は,前提を誤るものとして失当である。
(3)原告が主張する各技術常識が存在しなかったことは,前記(2)において説示したとおりであるから,これを前提とした上,本件明細書の発明の詳細な説明において,本件化合物が「痛みの処置における鎮痛剤」の用途に使用できることにつき薬理データ又はこれと同視し得る程度の事項が記載され,本件出願日当時の当業者において,本件化合物が当該用途の医薬として使用できることを理解できたかについて検討する。
ア 前記1(2)ア(ア)d,e及びgのとおり,本件明細書には,薬理データ又はこれと同視し得る程度の事項として,本件化合物がホルマリン試験,カラゲニン試験及び術後疼痛試験において効果を奏した旨の記載がある。しかしながら,前記(2)エにおいて説示したとおり,本件出願日当時,ホルマリン試験の後期相が専ら中枢性感作を反映するものであるとの技術常識並びにカラゲニン試験及び術後疼痛試験が神経の機能異常に基づく痛覚過敏や接触異痛の痛みを反映するものであるとの技術常識は存在せず,また,前記(2)オにおいて説示したとおり,本件出願日当時,痛みを原因によって区別できないとの技術常識も存在しなかったから,本件化合物がホルマリン試験,カラゲニン試験及び術後疼痛試験において引き起こされた各痛みの処置において効果を奏した旨の記載があるからといって,そのことをもって,当業者において,本件化合物が原因を異にするあらゆる「痛み」の処置においても効果を奏すると理解したとは到底いえない。したがって,ホルマリン試験,カラゲニン試験及び術後疼痛試験の結果に係る上記記載をもって,本件明細書の発明の詳細な説明において,本件化合物が「痛みの処置における鎮痛剤」の用途に使用できることにつき薬理データ又はこれと同視し得る程度の事項が記載され,本件出願日当時の当業者において,本件化合物が当該用途の医薬として使用できることを理解できたと認めることはできない。
イ なお,前記1(2)ア(ア)fのとおり,本件明細書には,ベネットモデル及びチャングモデルへの言及があるが,本件化合物がベネットモデル及びチャングモデルにおいてどのような結果を示したのかについての記載は全くないから,本件明細書におけるベネットモデル及びチャングモデルへの言及をもって,薬理データ又はこれと同視し得る程度の記載であるとみることはできない。
ウ また,原告は,本件明細書には,①本件化合物が「抗痛覚過敏作用」を有するものであること,②本件化合物が慢性疼痛に対して効果を奏するものであること,③本件化合物が神経障害性疼痛を生ずる様々な疾患(線維筋痛症を含む。)の痛みに使用できること,④本件化合物を麻薬性鎮痛剤やNSAIDに代わる新規の鎮痛剤として提案することが記載されているとも主張するが,これらの記載をもって,薬理データ又はこれと同視し得る程度の記載であるとみることはできない。
エ その他,本件明細書の発明の詳細な説明に,本件化合物が「痛みの処置における鎮痛剤」の用途に使用できることにつき,薬理データ又はこれと同視し得る程度の事項が記載され,本件出願日当時の当業者において,本件化合物が当該用途の医薬として使用できることを理解できたと認めるに足りる的確な証拠はない。
(4)原告のその余の主張について
ア 原告は,医学専門家作成の陳述書(甲67~69)の記載を採用せず,痛覚過敏や接触異痛の痛みが中枢性感作によって生じること,本件明細書に記載されたホルマリン試験,カラゲニン試験及び術後疼痛試験が痛覚過敏や接触異痛の痛みに対する薬剤の効果を確かめる試験として周知であったことなどの技術常識を認定しなかった本件審決は誤りであると主張する。
・・・
イ 原告は,症状に着目した動物モデルを基に実施可能要件を具備するものとして登録がされた先例特許の存在や審査ハンドブックの記載は本件明細書の発明の詳細な説明の記載が本件各発明について実施可能要件を満たさないとの結論を左右しないとした本件審決の判断は誤りであると主張するが,原告が主張する先例特許の存否及び内容や審査ハンドブックの記載内容はともかく,原告の主張は,本件明細書の発明の詳細な説明の記載自体が本件各発明について実施可能要件を満たす旨をいうものではないから,主張自体失当である。
ウ 原告は,本件各発明は技術進歩の著しい分野におけるいわゆるパイオニア発明であるところ,そのような発明については,実施可能要件等の記載要件を厳格に適用するのは相当でないし,記載要件を満たすか否かにつきわずかな疑義があることを理由として当該発明に係る特許を無効とするのは誤りであると主張するが,本件各発明が原告の主張するようなパイオニア発明であるか否かはともかく,実施可能要件やサポート要件は,特許法が規定する独占的権利を付与する前提として課されるものであるから,パイオニア発明についてはその厳格な適用を回避すべきであるなどと解することはできない。原告の主張は,独自の見解であり,採用することができない(なお,前記(1)ないし(3)において説示したところに照らすと,本件は,実施可能要件を満たすか否かにつきわずかな疑義があるにすぎない事案ではない。)。
(5)小括
以上のとおりであるから,本件明細書の発明の詳細な説明の記載が本件各発明について実施可能要件を満たさないとした本件審決の判断に誤りはない。取消事由2は理由がない。
3 取消事由3(サポート要件についての判断の誤り)について
(1)特許請求の範囲の記載がサポート要件(平成14年法律第24号による改正前の特許法36条6項1号)を満たすか否かは,特許請求の範囲の記載と発明の詳細な説明の記載とを対比し,特許請求の範囲に記載された発明が発明の詳細な説明に記載された発明であって,発明の詳細な説明の記載により当業者が当該発明の課題を解決できると認識できる範囲のものであるか否か,また,その記載や示唆がなくても当業者が出願時の技術常識に照らし当該発明の課題を解決できると認識できる範囲のものであるか否かを検討して判断するのが相当である(知財高裁平成17年(行ケ)第10042号同年11月11日判決)。
(2)特許請求の範囲の記載(前記第2の2)及び本件明細書の記載(前記1(2)ア(ア))によると,本件各発明は,本件化合物を「痛みの処置における鎮痛剤」として提供することを課題とするものであると認められる。
そして,前記2において説示したところに照らすと,本件各発明は,本件明細書の発明の詳細な説明の記載により当業者が上記課題を解決できると認識できる範囲のものであるとはいえず,かつ,当業者が本件出願日当時の技術常識に照らし上記課題を解決できると認識できる範囲のものであるともいえない。
そうすると,本件各発明に係る特許請求の範囲の記載は,サポート要件を満たさないというべきである。
(3)小括
したがって,本件各発明に係る特許請求の範囲の記載がサポート要件を満たさないとした本件審決の判断に誤りはない。取消事由3は理由がない。
4 結論
以上の次第であるから,原告の請求は理由がない。
1 取消事由1(本件訂正についての判断の誤り)について
(1)訂正の要件(新規事項の追加)について
ア 原告は,本件化合物2につき神経障害や線維筋痛症による痛覚過敏や接触異痛の痛みに対して「効果を奏すること」を当業者が理解できるか否かは実施可能要件等の記載要件に係る判断において検討すべき事柄であるから,本件化合物2につき神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置に鎮痛剤として「有効であること」が記載されているに等しいと当業者が理解するとはいえないとして訂正事項2-2に係る本件訂正が新規事項の追加に当たると判断した本件審決は特許法134条の2第9項において準用する同法126条5項の適用を誤るものであると主張する。
イ 特許無効審判における訂正の請求は,「願書に添付した明細書,特許請求の範囲又は図面に記載した事項の範囲内において」しなければならず(特許法134条の2第9項において準用する同法126条5項),同事項とは,当業者によって,明細書,特許請求の範囲又は図面の全ての記載を総合することにより導かれる技術的事項であり,訂正が,このようにして導かれる技術的事項との関係において,新たな技術的事項を導入しないものであるときは,当該訂正は,いわゆる新規事項の追加とならず,「明細書,特許請求の範囲又は図面に記載した事項の範囲内において」するものということができる(知財高裁平成18年(行ケ)第10563号同20年5月30日判決参照)。
しかるところ,本件発明2は,公知の物質である本件化合物2について鎮痛剤としての医薬用途を見出したとするいわゆる医薬用途発明であるところ,訂正事項2-2に係る本件訂正は,「請求項1記載の(鎮痛剤)」とあるのを「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛みの処置における(鎮痛剤)」に訂正するというものであり,鎮痛剤としての用途を具体的に特定することを求めるものである。そして,「痛みの処置における鎮痛剤」が医薬用途発明たり得るためには,当該鎮痛剤が当該痛みの処置において有効であることが当然に求められるのであるから,訂正事項2-2に係る本件訂正が新規事項の追加に当たらないというためには,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置における鎮痛剤として「効果を奏すること」が,当業者によって,本件出願日当時の技術常識も考慮して,本件明細書(本件訂正前の特許請求の範囲を含む。以下同じ。)又は図面の全ての記載を総合することにより導かれる技術的事項として存在しなければならないことになる。
ウ この点に関し,原告は,新規事項の追加に当たるか否かの判断においては,訂正事項が当業者によって明細書又は図面の全ての記載を総合することにより導かれる技術的事項であるか否かが検討されれば足りることから,本件審決の判断には誤りがあると主張する。しかしながら,上記のとおりの本件発明2の内容及び訂正事項2-2の内容に照らせば,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置に「効果を奏すること」が本件明細書又は図面の記載から導かれなければ,訂正事項2-2につき,これが当業者によって本件明細書又は図面の全ての記載を総合することにより導かれる技術的事項であるとはいえない。したがって,原告の上記主張を前提にしても,訂正事項2-2に係る本件訂正が新規事項の追加に当たらないというためには,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置における鎮痛剤として「効果を奏すること」が本件明細書又は図面に記載されているか,記載されているに等しいと当業者が理解するといえなければならないというべきである。
エ したがって,訂正事項2-2に係る本件訂正が新規事項の追加に当たらないというためには,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置における鎮痛剤として「効果を奏すること」が本件明細書に記載されているか,記載されているに等しいと当業者が理解するといえなければならないというべきであるとした本件審決(なお,本件審決は,本件訂正の許否の判断において,本件明細書に加えて図面の記載についても検討しており,本件審決のいう「明細書」は図面を含む趣旨と解される。)は,特許法134条の2第9項において準用する同法126条5項の適用を誤るものではない。
(2)訂正事項2-2に係る本件訂正が願書に添付した明細書又は図面に記載した事項の範囲内の訂正であるとの原告の主張について
本件審決が判断した順序に従い,まず,訂正事項2-2に係る本件訂正について判断する。
ア 本件化合物2が「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛み」の処置において効果を奏することにつき本件明細書又は図面に明示の記載があるかについて
(ア)本件明細書及び図面の記載
・・・
(イ)検討
a(a)前記(ア)bのとおり,本件明細書には,発明の概要として,本件化合物2が使用される疼痛性障害の中に神経障害及び線維筋痛症が含まれる旨の記載があるが,この部分には,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない(なお,本件化合物2が使用される疼痛性障害の中に神経障害及び線維筋痛症が含まれるとの一般的な記載があっても,そのことから,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏すると解することはできない。)。
(b)前記(ア)cのとおり,本件明細書には,発明の詳述として,本件化合物2が鎮痛剤として使用される対象の痛みに神経障害の痛みが含まれる旨の記載があるが,この部分にも,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない。
(c)前記(ア)dのとおり,本件明細書には,ホルマリン試験に関し,本件化合物2がホルマリン試験の後期相において効果を奏し,初期相においては影響がなかった旨の記載があるが,この部分にも,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない。
(d)前記(ア)eのとおり,本件明細書には,カラゲニン試験に関し,本件化合物2が機械的痛覚過敏及び熱痛覚過敏の痛みに対して効果を奏した旨の記載があるが,この部分にも,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない(なお,本件明細書の当該部分には,本件化合物2が「炎症性疼痛」の処置に有効であることを示す旨の記載がある。)。
(e)前記(ア)gのとおり,本件明細書には,術後疼痛試験に関し,本件化合物2が熱痛覚過敏及び接触異痛の痛みに対して効果を奏した旨の記載があるが,この部分にも,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載はない。
(f)その他,本件明細書及び図面には,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は接触異痛の痛みの処置において効果を奏する旨の記載がないから,本件明細書及び図面には,その旨の明示の記載がないと認めるのが相当である。
b この点に関し,原告は,本件明細書には,ホルマリン試験において中枢性感作及びこれによる痛覚過敏や接触異痛の痛みを反映する後期相に対する本件化合物2の効果が確かめられている旨,カラゲニン試験において痛覚過敏の痛みに対する本件化合物2の効果が確かめられている旨並びに術後疼痛試験において痛覚過敏及び接触異痛の痛みに対する本件化合物2の効果が確かめられている旨の記載があるから,本件明細書には,本件化合物2を痛覚過敏や接触異痛の痛みに対して用いることも,神経障害性疼痛や線維筋痛症に対して用いることも明示されていると主張する。
しかしながら,ホルマリン試験の後期相が中枢性感作及びこれによる痛覚過敏や接触異痛の痛みを反映するものであることが本件出願日当時の技術常識であったとの原告の主張が認められないことは,後記イ(ア)bにおいて説示するとおりであるし,前記a(c)ないし(e)において説示したところに照らすと,ホルマリン試験,カラゲニン試験及び術後疼痛試験の結果に係る記載を考慮しても,本件化合物2が神経障害又は線維筋痛症による痛覚過敏又は線維筋痛症の痛みの処置において効果を奏することが本件明細書又は図面に明示されていると認めることはできない。原告の上記主張は,採用することができない。
イ 本件化合物2が「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛み」の処置において効果を奏することが本件明細書又は図面に記載されているに等しいと本件出願日当時の当業者が理解したといえるかについて
(ア)原告が主張する本件出願日当時の技術常識の存否について
原告は,本件化合物2が「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛み」の処置において効果を奏することが本件明細書に明記されていないとしても,本件出願日当時の技術常識に照らせば,これが記載されているに等しいと当業者は理解したといえるとして,様々な技術常識の存在について主張し,また,これを認定しなかった本件審決が誤りであると主張するので,以下,原告が主張する技術常識の存否について順次検討する。
・・・
(イ)原告が主張する各技術常識が存在しなかったことは,前記(ア)において説示したとおりであるから,これを前提に,本件出願日当時の当業者において,本件化合物2が「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛み」の処置において効果を奏することが本件明細書又は図面に記載されているに等しいと理解したといえるかについて以下検討する。
a 原告は,ホルマリン試験によって引き起こされた後期相に本件化合物2を用いることにより効果が確認された旨の本件明細書の記載を根拠に,痛覚過敏及び接触異痛の痛みの処置に本件化合物2を用いることは,本件明細書の記載から自明であると主張する。
原告の上記主張は,本件出願日当時にホルマリン試験の後期相が中枢性感作によって生じる痛覚過敏及び接触異痛の痛みに対する薬剤の効果を確認する試験として広く知られていたことを根拠とするものである。しかしながら,前記(ア)bにおいて説示したとおり,ホルマリン試験の後期相が専ら中枢性感作を反映したものであることや,ホルマリン試験が痛覚過敏及び接触異痛の痛みに対する薬剤の効果を確認するための試験であることが本件出願日当時の技術常識であったと認めることはできないから,原告の上記主張は,その根拠を欠くものといわざるを得ない。
・・・
ウ 以上のとおりであるから,訂正事項2-2に係る本件訂正が願書に添付した明細書又は図面に記載した事項の範囲内の訂正であるということはできない。したがって,訂正事項2-2に係る本件訂正は,特許法134条の2第9項において準用する同法126条5項に違反し,許されない。
(3)訂正事項2に係る本件訂正について
訂正事項2-2に係る本件訂正が許されないことは,前記(2)において説示したとおりであるから,訂正事項2-2を含む訂正事項2に係る本件訂正も,特許法134条の2第9項において準用する同法126条5項に違反し,許されない。これと同旨の本件審決の判断に誤りはない。
(4)訂正事項1に係る本件訂正について
本件訂正前の請求項1及び2は,請求項2が請求項1の記載を引用する関係にあるから,請求項1及び2に係る本件訂正(訂正事項1及び2に係る本件訂正)は,一群の請求項1及び2についてされるものであるところ,前記(3)において説示したとおり,訂正事項2に係る本件訂正は許されないから,請求項2と共に一群の請求項を構成する請求項1に係る本件訂正(訂正事項1に係る本件訂正)も,許されない。これと同旨の本件審決の判断に誤りはない(なお,原告も,請求項2に係る本件訂正(訂正事項2に係る本件訂正)が許されない場合には,請求項2と共に一群の請求項を構成する請求項1に係る本件訂正(訂正事項1に係る本件訂正)も許されないことになることを争うものではない。)。
(5)小括
以上のとおり,訂正事項1及び2に係る本件訂正を許さなかった本件審決の判断に誤りはない。取消事由1は理由がない。
2 取消事由2(実施可能要件についての判断の誤り)について
(1)平成14年法律第24号による改正前の特許法36条4項は,明細書の発明の詳細な説明は,その発明の属する技術の分野における通常の知識を有する者がその実施をすることができる程度に明確かつ十分に記載しなければならないと定めるところ,この規定にいう「実施」とは,物の発明については,その物の使用等をする行為をいうのであるから(特許法2条3項1号),物の発明について実施可能要件を満たすためには,明細書の発明の詳細な説明の記載が,当業者において,その記載及び出願時の技術常識に基づいて,過度の試行錯誤を要することなく,当該発明に係る物を使用することができる程度のものでなければならない。
そして,医薬用途発明においては,一般に,物質名,化学構造等が示されることのみによっては,その有用性を予測することは困難であり,発明の詳細な説明に,医薬の有効量,投与方法等が記載されていても,それだけでは,当業者において当該医薬が実際にその用途において使用できるかを予測することは困難であるから,当業者が過度の試行錯誤を要することなく当該発明に係る物を使用することができる程度の記載があるというためには,明細書において,当該物質が当該用途に使用できることにつき薬理データ又はこれと同視することができる程度の事項を記載し,出願時の技術常識に照らして,当該物質が当該用途の医薬として使用できることを当業者が理解できるようにする必要があると解するのが相当である。
これを本件についてみると,本件各発明は,前記第2の2のとおり,本件化合物を「痛みの処置における鎮痛剤」の用途に使用する医薬用途発明であるから,本件各発明について本件明細書の発明の詳細な説明の記載が実施可能要件を満たすといえるためには,本件明細書において,本件化合物が「痛みの処置における鎮痛剤」の用途に使用できることにつき薬理データ又はこれと同視することができる程度の事項を記載し,本件出願日当時の技術常識に照らして,本件化合物が当該用途の医薬として使用できることを当業者が理解できるようにする必要がある。
(2)原告は,本件明細書の記載に加え,本件出願日当時の技術常識を併せ考慮すれば,本件明細書の記載を見た当業者は本件化合物が原因にかかわらず痛覚過敏や接触異痛の痛みに対して効果を奏するものと理解し,また,本件化合物が少なくとも神経障害や線維筋痛症による痛覚過敏や接触異痛の痛みに対して効果を奏するものと理解するといえるとして,本件明細書の発明の詳細な説明が本件各発明について実施可能要件を満たすと主張するので,まず,原告が主張する技術常識の存否について,以下検討する(もっとも,前記(1)のとおり,本件各発明は,「痛み」の処置における鎮痛剤の用途に使用されるものであり,当該「痛み」には何らの特定もされていないのであるから,実施可能要件を満たすか否かを判断するに当たって検討すべき本件出願日当時の当業者の理解の対象は,本件化合物が「痛覚過敏や接触異痛の痛み」又は「神経障害や線維筋痛症による痛覚過敏や接触異痛の痛み」に対して効果を奏することではなく,本件化合物が「痛み」に対して効果を奏することである。)。
ア 原告は,神経障害性疼痛や線維筋痛症による痛覚過敏や接触異痛の痛みはその原因にかかわらず抹消や中枢の神経細胞の感作によって生じることが本件出願日当時に知られていたと主張するが,そのような事実が認められないことは,前記1(2)イ(ア)aにおいて説示したとおりである。
なお,原告は,特発性疼痛についても,神経細胞の感作により痛みの症状が生じるものであると主張するが,前記1(2)イ(ア)aにおいて説示したところに照らすと,そのような事実を認めることはできず,その他,そのような事実を認めるに足りる的確な証拠はない。
イ 原告は,中枢性感作に対して効果を奏するケタミンが原因にかかわらず痛覚過敏や接触異痛の痛みに対して効果があることが本件出願日当時に知られていたと主張するが,そのような事実が認められないことは,前記1(2)イ(ア)eにおいて説示したとおりである。
ウ 原告は,上記ア及びイの技術常識が存在したことを根拠に,本件出願日当時の当業者は痛みに共通の治療法があることを理解していたと主張するが,上記ア及びイの技術常識は認められないから,原告の主張は根拠を欠くものとして失当である。
エ 原告は,本件出願日当時,ホルマリン試験の後期相は中枢性感作を反映するものであるとの技術常識が存在し,これは仮説ではなかったと主張するが,ホルマリン試験の後期相が専ら中枢性感作を反映したものであることが技術常識であったと認めることができないことは,前記1(2)イ(ア)bにおいて説示したとおりである。
なお,原告は,カラゲニン試験及び術後疼痛試験についても,神経の機能異常に基づく痛覚過敏や接触異痛の痛みを反映するものであったと主張するが,前記1(2)イ(ア)a及びcにおいて説示したところに照らすと,そのような事実を認めることはできず,その他,そのような事実を認めるに足りる的確な証拠はない。オ原告は,痛みを原因によって区別できないことは本件出願日当時の技術常識であったと主張するが,そのような技術常識が認められないことは,前記1(2)イ(ア)fにおいて説示したとおりである。
カ 原告は,本件出願日当時の当業者は疼痛の原因にかかわらず,痛覚過敏や接触異痛の痛みを発現する動物モデル試験で特定の化合物の効果を確認できれば,その動物モデル試験におけるのとは別の原因によって生じた痛覚過敏や接触異痛の痛みに対しても当該化合物が同様に効果を奏するものと理解していたと主張するが,原告の主張が前提を欠き失当であることは,前記1(2)イ(ア)f(d)において説示したとおりである。
キ なお,原告は,本件明細書においてベネットモデルやチャングモデルへの言及があれば,本件出願日当時の当業者は炎症や手術とは異なる原因によって生じた痛覚過敏や接触異痛の痛みに対しても本件化合物が有用であることを十分に理解できたと主張する。しかしながら,前記1(2)ア(ア)fのとおり,本件明細書には,ベネットモデル及びチャングモデルについて,「BennetG.J.のアッセイはヒトに認められるのと類似の疼痛感覚の障害を生じるラットにおける末梢性単発神経障害の動物モデルを提供する(Pain,1988;33:87-107)。KimS.H.らのアッセイは,ラットにおける分節脊椎神経の結紮によって生じる末梢神経障害の一つの実験モデルを提供する(Pain,1990;50:355-363)。」との記載があるのみであり,本件化合物がベネットモデルやチャングモデルにおいてどのような結果を示したのかについての記載は全くないから,上記記載をもって,本件出願日当時の当業者が炎症や手術とは異なる原因によって生じた痛覚過敏や接触異痛の痛みに対しても本件化合物が有用であることを理解できたと認めることはできない。
この点に関し,原告は,本件出願日後の文献である甲28の文献(Elsevier Science B.V.発行の「pain 83」(1999年)に掲載された「Detection of static and dynamic components of mechanical allodynia in rat models of neuropathic pain: are they signaled by distinct primary sensory neurons?」(Mark J. Fieldら著))の記載は本件化合物が実際にベネットモデルやチャングモデルにおいて効果を奏したことを裏付けるものであるから,これを参酌すべきであると主張するが,上記のとおり,本件明細書には,本件化合物がベネットモデルやチャングモデルにおいて効果を奏した旨の記載が全くないのであるから,甲28の文献の記載が本件明細書の記載内容を裏付けるとはいえない。原告の主張は,前提を誤るものとして失当である。
(3)原告が主張する各技術常識が存在しなかったことは,前記(2)において説示したとおりであるから,これを前提とした上,本件明細書の発明の詳細な説明において,本件化合物が「痛みの処置における鎮痛剤」の用途に使用できることにつき薬理データ又はこれと同視し得る程度の事項が記載され,本件出願日当時の当業者において,本件化合物が当該用途の医薬として使用できることを理解できたかについて検討する。
ア 前記1(2)ア(ア)d,e及びgのとおり,本件明細書には,薬理データ又はこれと同視し得る程度の事項として,本件化合物がホルマリン試験,カラゲニン試験及び術後疼痛試験において効果を奏した旨の記載がある。しかしながら,前記(2)エにおいて説示したとおり,本件出願日当時,ホルマリン試験の後期相が専ら中枢性感作を反映するものであるとの技術常識並びにカラゲニン試験及び術後疼痛試験が神経の機能異常に基づく痛覚過敏や接触異痛の痛みを反映するものであるとの技術常識は存在せず,また,前記(2)オにおいて説示したとおり,本件出願日当時,痛みを原因によって区別できないとの技術常識も存在しなかったから,本件化合物がホルマリン試験,カラゲニン試験及び術後疼痛試験において引き起こされた各痛みの処置において効果を奏した旨の記載があるからといって,そのことをもって,当業者において,本件化合物が原因を異にするあらゆる「痛み」の処置においても効果を奏すると理解したとは到底いえない。したがって,ホルマリン試験,カラゲニン試験及び術後疼痛試験の結果に係る上記記載をもって,本件明細書の発明の詳細な説明において,本件化合物が「痛みの処置における鎮痛剤」の用途に使用できることにつき薬理データ又はこれと同視し得る程度の事項が記載され,本件出願日当時の当業者において,本件化合物が当該用途の医薬として使用できることを理解できたと認めることはできない。
イ なお,前記1(2)ア(ア)fのとおり,本件明細書には,ベネットモデル及びチャングモデルへの言及があるが,本件化合物がベネットモデル及びチャングモデルにおいてどのような結果を示したのかについての記載は全くないから,本件明細書におけるベネットモデル及びチャングモデルへの言及をもって,薬理データ又はこれと同視し得る程度の記載であるとみることはできない。
ウ また,原告は,本件明細書には,①本件化合物が「抗痛覚過敏作用」を有するものであること,②本件化合物が慢性疼痛に対して効果を奏するものであること,③本件化合物が神経障害性疼痛を生ずる様々な疾患(線維筋痛症を含む。)の痛みに使用できること,④本件化合物を麻薬性鎮痛剤やNSAIDに代わる新規の鎮痛剤として提案することが記載されているとも主張するが,これらの記載をもって,薬理データ又はこれと同視し得る程度の記載であるとみることはできない。
エ その他,本件明細書の発明の詳細な説明に,本件化合物が「痛みの処置における鎮痛剤」の用途に使用できることにつき,薬理データ又はこれと同視し得る程度の事項が記載され,本件出願日当時の当業者において,本件化合物が当該用途の医薬として使用できることを理解できたと認めるに足りる的確な証拠はない。
(4)原告のその余の主張について
ア 原告は,医学専門家作成の陳述書(甲67~69)の記載を採用せず,痛覚過敏や接触異痛の痛みが中枢性感作によって生じること,本件明細書に記載されたホルマリン試験,カラゲニン試験及び術後疼痛試験が痛覚過敏や接触異痛の痛みに対する薬剤の効果を確かめる試験として周知であったことなどの技術常識を認定しなかった本件審決は誤りであると主張する。
・・・
イ 原告は,症状に着目した動物モデルを基に実施可能要件を具備するものとして登録がされた先例特許の存在や審査ハンドブックの記載は本件明細書の発明の詳細な説明の記載が本件各発明について実施可能要件を満たさないとの結論を左右しないとした本件審決の判断は誤りであると主張するが,原告が主張する先例特許の存否及び内容や審査ハンドブックの記載内容はともかく,原告の主張は,本件明細書の発明の詳細な説明の記載自体が本件各発明について実施可能要件を満たす旨をいうものではないから,主張自体失当である。
ウ 原告は,本件各発明は技術進歩の著しい分野におけるいわゆるパイオニア発明であるところ,そのような発明については,実施可能要件等の記載要件を厳格に適用するのは相当でないし,記載要件を満たすか否かにつきわずかな疑義があることを理由として当該発明に係る特許を無効とするのは誤りであると主張するが,本件各発明が原告の主張するようなパイオニア発明であるか否かはともかく,実施可能要件やサポート要件は,特許法が規定する独占的権利を付与する前提として課されるものであるから,パイオニア発明についてはその厳格な適用を回避すべきであるなどと解することはできない。原告の主張は,独自の見解であり,採用することができない(なお,前記(1)ないし(3)において説示したところに照らすと,本件は,実施可能要件を満たすか否かにつきわずかな疑義があるにすぎない事案ではない。)。
(5)小括
以上のとおりであるから,本件明細書の発明の詳細な説明の記載が本件各発明について実施可能要件を満たさないとした本件審決の判断に誤りはない。取消事由2は理由がない。
3 取消事由3(サポート要件についての判断の誤り)について
(1)特許請求の範囲の記載がサポート要件(平成14年法律第24号による改正前の特許法36条6項1号)を満たすか否かは,特許請求の範囲の記載と発明の詳細な説明の記載とを対比し,特許請求の範囲に記載された発明が発明の詳細な説明に記載された発明であって,発明の詳細な説明の記載により当業者が当該発明の課題を解決できると認識できる範囲のものであるか否か,また,その記載や示唆がなくても当業者が出願時の技術常識に照らし当該発明の課題を解決できると認識できる範囲のものであるか否かを検討して判断するのが相当である(知財高裁平成17年(行ケ)第10042号同年11月11日判決)。
(2)特許請求の範囲の記載(前記第2の2)及び本件明細書の記載(前記1(2)ア(ア))によると,本件各発明は,本件化合物を「痛みの処置における鎮痛剤」として提供することを課題とするものであると認められる。
そして,前記2において説示したところに照らすと,本件各発明は,本件明細書の発明の詳細な説明の記載により当業者が上記課題を解決できると認識できる範囲のものであるとはいえず,かつ,当業者が本件出願日当時の技術常識に照らし上記課題を解決できると認識できる範囲のものであるともいえない。
そうすると,本件各発明に係る特許請求の範囲の記載は,サポート要件を満たさないというべきである。
(3)小括
したがって,本件各発明に係る特許請求の範囲の記載がサポート要件を満たさないとした本件審決の判断に誤りはない。取消事由3は理由がない。
4 結論
以上の次第であるから,原告の請求は理由がない。
コメント