<判決紹介>
平成25年(ワ)第33993号 特許権侵害差止等請求事件■コメント
結晶特許に関する新薬vsジェネリックの侵害訴訟。 先発品はリバロ(一般名:ピタバスタチンカルシウム)。
被告製品の15本のピークの回折角のうち、9本がクレームの回折角(構成要件C・C’)と一致していなかった。 原告は以下の点を主張したが認められなかった。 構成要件非充足。 ☆☆
(1)クレームの回折角の数値は結晶形態Aとの同一性を判断するための数値にすぎない。
(2)同一性の判断は、日本薬局方等によれば、X線粉末回折法において±0.2°以内の誤差で一致するピークが10本以上確認されるなどすれば十分である。別紙原告測定結果によれば,被告製品は10本以上確認されており、構成要件C・C’を充足する。■抜粋
・平成25年(ワ)第33993号 特許権侵害差止等請求事件
・平成27年1月27日判決言渡、東京地方裁判所民事第29部
・原告: 日産化学工業株式会社
・原告補助参加人: 興和株式会社
・被告: ダイト株式会社、持田製薬株式会社、東和薬品株式会社、鶴原製薬株式会社、科研製薬株式会社、小林化工株式会社、Meiji Seika
・特許: 特許5186108、5267643
・請求項:
【請求項1】:特許5186108
A 式(1)で表される化合物であり,
【化1】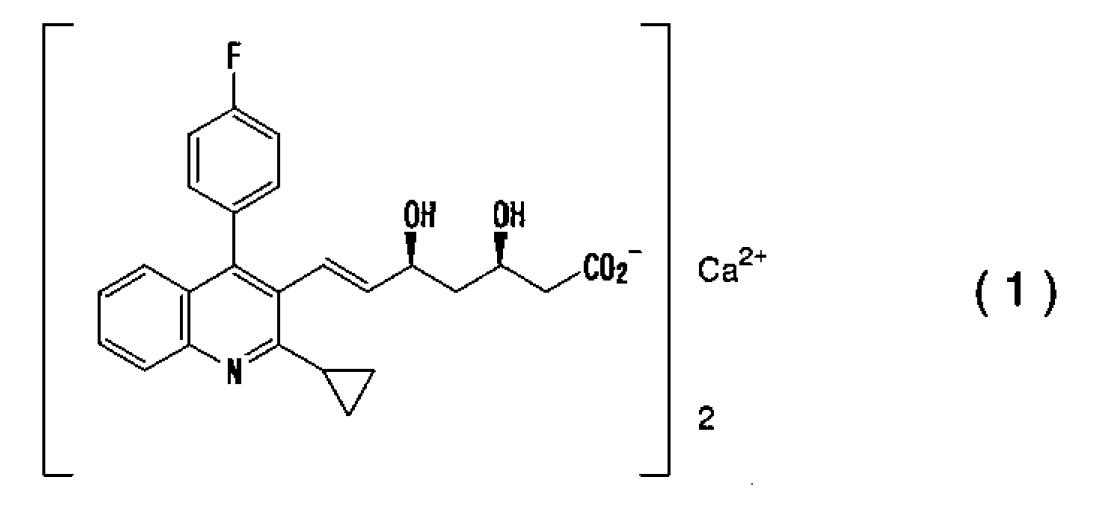
B 7~13%の水分を含み,
C CuKα放射線を使用して測定するX線粉末解析において,4.96°,6.72°,9.08°,10.40°,10.88°13.20°,13.60°,13.96°,18.32°,
20.68°,21.52°,23.64°,24.12°及び27.00°の回折角(2θ)にピークを有し,かつ,30.16°の回折角(2θ)に,20.68°の回折角(2θ)のピーク強度を100%とした場合の相対強度が25%より大きなピークを有することを特徴とする
D ピタバスタチンカルシウム塩の結晶
E (但し,示差走査熱量測定による融点95℃を有するものを除く)。
【請求項1】:特許5267643
C’ CuKα放射線を使用して測定するX線粉末解析において,4. 96°,6.72°,9.08°,
10.40°,10.88°,13. 20°,13.60°,13.96°,18.32°,20.68°, 21.52°,23.64°,24.12°,27.00°及び30. 16°の回折角(2θ)にピークを有し,かつ
B 7重量%~13重量%の水分を含む,
A 式(1)で表される
【化1】
D ピタバスタチンカルシウム塩の結晶
E (但し,示差走査熱量測定による融点95℃を有するものを除く)を,
H その含有水分が4重量%より多く,15重量%以下の量に維持することを特徴とする
I ピタバスタチンカルシウム塩の保存方法。
・概要
第2 事案の概要
本件は,ピタバスタチンカルシウム塩の結晶及びその保存方法に関する2件の特許権を有する原告が,被告らによる原薬及び製剤の製造・販売等が上記各特許権の侵害に当たる旨主張して,特許法100条1項に基づきその差止めを求める事案である。
1 前提事実(後掲各証拠及び弁論の全趣旨により容易に認められる事実を含む。なお,特に断らない限り,証拠の枝番号の記載は省略する。以下同じ。)
(1) 当事者原告は,基礎化学品,医薬品の製造・販売等を業とする株式会社である。被告ダイトは,医薬品製剤の原薬,医薬品の製造・販売等を業とする株式会社であり,その余の被告らは,いずれも医薬品の製造・販売等を業とする株式会社である。
・・・。
第3 当裁判所の判断
・・・。
(2) 前記前提事実及び上記認定事実に基づき,構成要件C・C’の回折角について検討する。
ア 本件各発明の構成要件C・C’においては,発明の構成が15本のピークの小数点以下2桁の回折角により特定されており,その数値に一定の誤差が許容される旨の記載や,15本中の一部のピークのみの対比によって特定される旨の記載はない。
また,上記認定の発明の詳細な説明の記載によれば,本件各発明は,ピタバスタチンカルシウム原薬に含まれる水分量を特定の範囲にコントロールすることでその安定性が格段に向上すること,及び,結晶形態A~Cの中で結晶形態Aが医薬品の原薬として最も好ましいことを見いだしたというものである。そして,結晶形態B及びCは,水分量が結晶形態Aと同等で,単に,CuKα放射線を使用して測定した粉末X線回折図で結晶形態Aに特徴的な3本のピークの回折角が存在しないことによって結晶形態Aと区別される結晶多形というのであるから,構成要件C・C’の小数点以下2桁の数値で表される15本のピーク中3本のみ相違することが,技術的範囲の属否を判別する根拠とされていることになる。
さらに,本件明細書のその余の記載をみても,結晶形態Aは構成要件C・C’の回折角等の粉末X線回折パターンによって特徴付けられるという以上の特定がされておらず(段落【0008】,【0010】,【0016】,【0033】参照。本件保存方法特許の明細書についても同様である。甲2の1及び2),回折角に一定の誤差が許容されることなどをうかがわせる記載も見当たらない。
そうすると,本件各発明の技術的範囲に属するというためには構成要件C・C’の回折角の数値が15本全てのピークについて小数点第2位まで一致することを要するというべきである。
イ 上記アの解釈は,前記(1)イ~エの事実からも裏付けられる。
すなわち,ピタバスタチンカルシウム塩の結晶形態には,本件明細書の結晶形態A~C及びチバ特許明細書の結晶多形A~F以外にも未知の結晶多形が存在し得るところ,粉末X線回折測定の回折角の数値により結晶形態を特定した医薬化合物の発明の特許出願には,ピークの回折角に±0.1°~0.2°の許容誤差を設けるものが多数存在し,結晶形態を特定するピークの本数も数本~十数本で特定するものなど多様であって,その技術的範囲が一定の許容誤差ないし一定のピーク本数によって判断されるとの技術常識は存在しないことがうかがわれるから,構成要件C・C’に記載された15本の数値のうち一部のみが一致し,又は一定の誤差の範囲で一致するにとどまる結晶がこれに含まれると解する場合には,本件各発明の技術的範囲への属否が一義的には定まらないこととなる。また,上記のように解すると,原告自身が本件各発明の技術的範囲に属しないことを認めている結晶形態までもがこれに属する結果になるなど(例えば,チバ特許明細書に記載の結晶形態Eは,構成要件C・C’に記載の15本のピークが全て±0.2°以内で一致する回折角を含んでいる。),不合理な結果となる。さらに,原告は,本件結晶特許の出願当初は1本のピークの回折角(許容誤差のない小数点以下2桁の数値)及び相対強度をもって発明を特定していたが,拒絶理由通知を受けて構成要件Cの回折角に係る補正をし,この補正が限定的減縮に当たる旨の意見を表明したのであるから,上記補正により,発明の技術的範囲を字義どおり小数点以下2桁の回折角の数値が15個全て一致する結晶に限定したとみるほかなく,このように解釈することが補正の趣旨に沿うものというべきである。
ウ 以上によれば,本件各発明の構成要件C・C’を充足するためには,15本のピークの全ての回折角の数値が小数点第2位まで一致することを要し,その全部又は一部が一致しないピタバスタチンカルシウム塩の結晶又はその保存方法はその技術的範囲に属するということができないものと解するのが相当である。
(3) これを被告原薬等についてみると,別紙原告測定結果の記載に被告らの主張するような問題点がある(甲5,27,55等によっても,原告がピークに当たると主張する角度の測定値がノイズではなくピークと判別される根拠が必ずしも明らかではない部分がある。)ことをおいても,原告測定においては,15本全てのピークについて回折角の数値が小数点第2位まで一致するような測定結果は得られなかったというのである(前記前提事実(3)エ)。そして,原告が被告原薬等に含まれるとするピタバスタチンカルシウム塩における15本のピークの回折角は別紙物件目録記載1のとおりであり,うち9本は構成要件C・C’と相違している。そうすると,同目録記載の回折角自体から,被告原薬等は構成要件C・C’を充足しないと判断すべきことになる。
(4) 以上の認定判断に対し,原告は,①本件発明の対象は本件明細書記載の結晶形態Aであり,その充足性は当該ピタバスタチンカルシウム塩の結晶の粉末X線回折測定で得られたチャートにおいて結晶形態Aとの同一性を判断するのに十分な数のピークが確認されれば足りる,②上記の同一性の判断は,日本薬局方等の記載によれば,X線粉末回折法において±0.2°以内の誤差で一致するピークが10本以上確認されるなどすれば十分である,③別紙原告測定結果によればモチダ錠及びこれに用いられた被告原薬は構成要件C・C’の回折角を充足すると主張する。
しかしながら,本件各発明の特許請求の範囲に結晶形態Aという記載はなく,また,前記発明の詳細な説明によっても,結晶形態Aとの同一性は構成要件C・C’の回折角の数値が全て一致するか否かにより判定すべきものと解されるから,構成要件C・C’の回折角の充足性は,端的に,当該結晶がその数値を全て充足するか否かにより判断すべきものであって,上記①の主張は失当である。
また,日本薬局方は,厚生労働大臣が医薬品の性状及び品質の適正を図るため,医薬品,医療機器等の品質,有効性及び安全性の確保等に関する法律41条(平成25年法律第84号による廃止前の薬事法41条も同趣旨)に基づき定める医薬品の規格基準書であり,原告の挙げる各文献中の記載も,上記法律の目的とする保健衛生の向上という公益的見地から医薬品の同一性等を判断する基準として記載されたものと解される。これに対し,医薬品等に係る特許発明の技術的範囲は,明細書の記載及び図面を考慮し当該発明に係る特許請求の範囲の記載に基づいて定めるべきものであるから(特許法70条1項,2項),日本薬局方の記載と常に一致しなければならないものではない。したがって,上記②の主張も理由がない。
さらに,上記③の主張は,原告の主張する回折角の解釈を前提とするものであるから,明らかに失当である。
(3) なお,本件結晶特許については本件訂正請求がされているが,構成要件C・C’の回折角は訂正の対象となっていないから,訂正の許否は本件の結論に影響するものではない。
判決文はこちらから
結晶特許において回折角が一致しないので非侵害と判断された事例
 結晶特許
結晶特許
コメント